Canakinumab (Ilaris®), un anticuerpo monoclonal (sufijo mab, de monoclonal anti-body) está indicado en el control de la artritis reumatoide juvenil y la artritis gotosa. Un reciente estudio (véase más adelante en este texto) ha mostrado que Canakinumab reduce el riesgo de ataques cardíacos e ictus, sobre todo en pacientes con historia clínica de enfermedad cardíaca. Así mismo, disminuye el riesgo de cáncer pulmonar.
El hallazgo ha abierto una nueva esperanza para los pacientes con enfermedad aterosclerótica que no responden de modo adecuado a los tratamientos convencionales.
La enfermedad cardíaca fue responsable de aproximadamente 15 millones de muertes en todo el mundo, 634.000 solo en Estados Unidos, 117.393 en España (año 2014). Canakinumab tiene dos problemas: de una parte sus efectos adversos, potencialmente mortales, derivados de la inhibición parcial del sistema inmune; y, de otro lado, su elevado coste, alrededor de $200,000 (dos cientos mil dólares) anualmente.
Canakinumab, de la multinacional helvética Novartis AG, fue autorizado para el tratamiento de la artritis reumatoide juvenil y otras patologías, pero no para la enfermedad cardíaca. Este estudio sobre la potencial eficacia de Canakinumab en la enfermedad aterosclerótica ha sido financiado por el fabricante, Novartis AG. No se ha informado si el coste del tratamiento sería similar caso de que se ampliasen sus indicaciones para incluir la «enfermedad cardíaca», una locución que engloba un conjunto de patologías de elevada prevalencia.
Canakinumab tiene un mecanismo de acción distinto al de las estatinas («inhibidores de la enzima metil-glutaril~CoA-reductasa»), desde hace muchos años el principal grupo farmacológico en que se sustenta el tratamiento de la aterosclerosis, consecuencia de elevados y persistentes niveles de Colesterol en plasma. A diferencia de las estatinas, Canakinumab no tiene efecto alguno sobre la concentración plasmática de colesterol.
Canakinumab reduce la inflamación. De esta observación (mejora de la función cardiovascular por acción anti-inflamatoria) se infiere el papel que la inflamación ejerce en procesos tan diversos como la función cardíaca e incluso el cáncer. Casi la mitad de las personas que sufren ataques cardíacos tienen niveles normales de colesterol. Tal vez en algunos, o todos, estos pacientes la inflamación pueda tener una influencia desdeñada hasta ahora en el abordaje terapéutico de estas enfermedades.
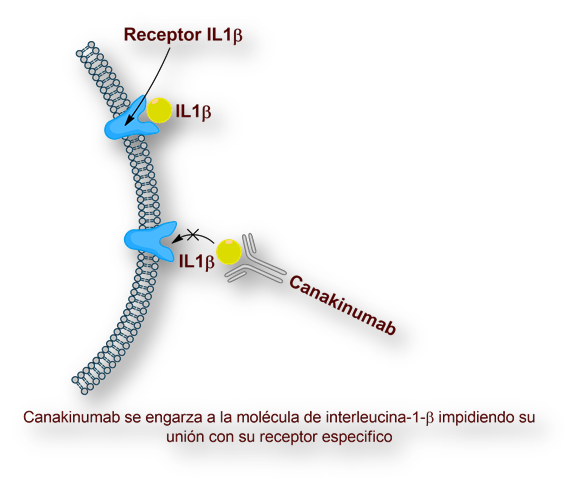
Canakinumab inhibe parcialmente la respuesta inmunitaria mediante el bloqueo de la interleucina-1β (ver imagen al inicio del artículo). La interleucina-1β, bloqueada por la unión del anticuerpo Canakinumab, no puede unirse a su receptor. [La interleucina-1β es un mediador de proceso inflamatorio y otros relacionados con la inmunidad].
La inhibición del sistema inmunitario, aunque parcial, es un factor de riesgo para la aparición de infecciones potencialmente mortales. En los estudios clínicos no se observó una diferencia estadísticamente significativa en la mortalidad entre los grupos de estudio (tratado con Canakinumab) y placebo. Muy probablemente, el incremento de mortandad por merma de actividad del sistema inmunitario se vio compensada por la reducción de la mortalidad de tipo cardiovascular.
Robert A. Harrington, de la universidad de Stanford (Estados Unidos) publicó una editorial en el mismo número de la revista The New England Journal of Medicine en que se publicaron los resultados del ensayo clínico. La editorial califica los resultados del estudio como «modestos», haciendo hincapié en las infecciones fatales asociadas al tratamiento. Estos aspectos, junto con el elevado coste del tratamiento con Canakinumab, entredicen la generalización de su prescripción en la enfermedad aterosclerótica, sobre todo cuando existen excelentes alternativas farmacológicas, mucho más baratas.
Canakinumab es mucho más potente y su efecto más rápido que los anti-inflamatorios clásicos, actuando por un mecanismo de acción diferente. Canakinumab inhibe a un «mediador de la inflamación», interleucina-1, bloqueando su engarce a receptores específicos.
Las estatinas ejercen también efectos anti-inflamatorios, pero muy limitados, sobre todo cuando se comparan con Canakinumab. En el estudio clínico que se acaba de dar a conocer solo se han incluido personas que tenían elevadas concentraciones de «proteína C-reactiva», un «marcador» de la inflamación, que estaban siendo tratadas con estatinas y que tenían niveles aceptables de LDL-Colesterol. [LDL, acrónimo en inglés de Low Density Lipoprotein]. [Se consideró elevada una concentración de «proteína C-reactiva» ≥ 2mg/L]. [Referencia bibliográfica sobre la proteína-C-reactiva: Ridker PM, Libby P. Risk Factors for Atherothrombotic Disease. In: Libby P, Bonow RO, Mann DL, Zipes DP, eds. Braunwald’s Heart Disease: A Textbook of Cardiovascular Medicine. 8th ed. Philadelphia, Pa; Saunders Elsevier; 2007: chap 39].
El estudio internacional involucró a 10.061 participantes de 39 países, con una edad promedio de 61 años, de las que un tercio eran mujeres; y un 40% diabéticos.
Los pacientes se distribuyeron de modo aleatorio. El brazo del estudio tratado con Canakinumab se distribuyó a su vez en tres subgrupos con escalado de dosificación. En todos los grupos la administración de Canakinumab fue trimestral. El grupo placebo recibía una inyección de aspecto similar, pero que contenía solo solución salina al 0,9%. Durante el estudio todos los pacientes (grupo placebo y grupo de estudio) continuaron con el tratamiento que tenían prescrito. La duración promedio del ensayo clínico fue de 3,7 años.
Las valoraciones parciales, realizadas anualmente, llegaron a las siguientes conclusiones: en el grupo placebo, 4,5 de cada 100 sufrieron ataque cardíaco, ictus o fallecieron por causa cardiovascular. La incidencia de accidentes cardiovasculares fue menor (3,86 de cada 100 participantes) en el grupo de estudio que recibió la dosis óptima de Canakinumab. Cuando se tuvo en cuenta la variable tiempo, la reducción de accidentes cardiovasculares fue del 15%.
El director del estudio ha sido Paul M. Ridker, del Center for Cardiovascular Disease Prevention del Brigham and Women’s Hospital, en Boston, Massachusetts, Estados Unidos.
Tal vez Canakinumab no acabe siendo un medicamento rutinario del tratamiento de la enfermedad aterosclerótica. Sin embargo, estos hallazgos consolidan una nueva vía de investigación, que relaciona la inflamación con la patología cardiovascular.
Si el medicamento llega a prescribirse para la enfermedad aterosclerótica, se restringirá a pacientes con elevadas concentraciones de «proteína-C-reactiva» («marcador» del proceso inflamatorio) y con historial clínico de ataques cardíacos o ictus. Este fue el criterio de inclusión en el estudio clínico. Además, los pacientes tratados deberían ser monitorizados ante cualquier signo de infección.
Por otra parte, Canakinumab evidenció una disminución de la incidencia, y la mortandad asociada, por cáncer de pulmón. No se tuvo constancia de que ningún participante padeciese cáncer de pulmón al inicio del estudio clínico. El cohorte tratado con las dosis más elevadas de Canakinumab mostró una disminución de la incidencia (dos tercios) y la mortandad (tres cuartos) debido a cáncer de pulmón. Sin embargo, esta observación fue incidental. No era el objetivo del estudio. Probablemente, este hallazgo dará pie para su estudio posterior con vistas a expandir las indicaciones de Canakinumab.
El estudio se presentó durante el simposio de la Sociedad Europea de Cardiología, que se ha desarrollado en Barcelona (agosto 2017).
Los resultados cardiovasculares de Canakinumab se han publicado en la revista norteamericana The New England Journal of Medicine; y los hallazgos sobre la reducción de la incidencia de cáncer de pulmón se han dado a conocer en la revista británica The Lancet.
Otro antiguo pero valioso medicamento, Metotrexato, también es sujeto de estudio por su posible eficacia a la hora de disminuir el riesgo cardiovascular. Metotrexto es un medicamento muy versátil, con múltiples indicaciones, muchas de ellas relacionadas con procesos inflamatorios crónicos, tales como artritis reumatoide, uveítis, enfermedad de Crohn. El estudio de la posible utilidad cardiovascular del Metotrexato es financiado por el gobierno federal norteamericano. Ningún laboratorio se muestra interesado porque el medicamento es muy barato; y, dada su antigüedad, no puede conseguir protección de patente.
Zaragoza, a 1 de septiembre de 2017
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Zaragoza