ANTIDEPRESIVO ADMINISTRACIÓN NASAL ESKETAMINA (SPRAVATO®)
Escáner cerebral (coloreado) de un enfermo con diagnóstico de depresión. Las regiones coloreadas en rojo muestran una irrigación sanguínea anormalmente baja.
El número de personas con diagnóstico de depresión crece continuamente, tal vez asociado a la mayor disponibilidad de tratamientos farmacológicos, tan bien tolerados como de eficacia dudosa a largo plazo.
El martes, 5 de marzo (2019), la Food and Drug Administration estadounidense aprobó el primer medicamento antidepresivo de acción rápida, en una formulación inhabitual para este tipo de medicamentos (spray nasal), dirigido a pacientes, bien refractarios a los tratamientos convencionales, o que precisen una respuesta urgente debido a su elevado riesgo de suicidio.
No se trata de un nuevo medicamento, sino de uno de los estereoisómeros (S) de un fármaco, la ketamina, usado desde hace muchos años como anestésico; y durante las décadas de 1980 y 1990 muy empleado ilegalmente con denominaciones como special K, y otros nombres, por sus efectos alucinatorios, descritos como «sensaciones extracorpóreas».
De hecho, es el primer medicamento antidepresivo que se comercializa desde hace muchos años.
 El nuevo antidepresivo es la esketamina (S-ketamina), formulado en spray nasal con el nombre registrado de Spravato® por laboratorios Janssen Pharmaceuticals Inc., una división de la multinacional Johnson & Johnson.
El nuevo antidepresivo es la esketamina (S-ketamina), formulado en spray nasal con el nombre registrado de Spravato® por laboratorios Janssen Pharmaceuticals Inc., una división de la multinacional Johnson & Johnson.
La ketamina, como antidepresivo, ya se administraba bajo criterios off-label en clínicas privadas en las que el paciente ingresaba durante unos días, pagando facturas, no reembolsables, superiores a los 5.000 euros.
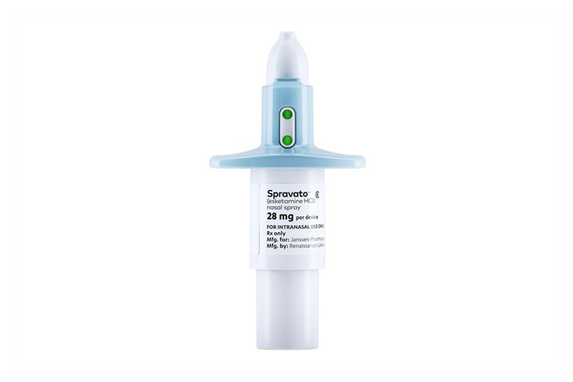 La comercialización de la esketamina (S-ketamina) regularizará esta situación, permitiendo que el coste de los tratamientos sea asumido por los servicios de salud públicos y privados. Además, podrá llevarse un control más riguroso de sus efectos adversos.
La comercialización de la esketamina (S-ketamina) regularizará esta situación, permitiendo que el coste de los tratamientos sea asumido por los servicios de salud públicos y privados. Además, podrá llevarse un control más riguroso de sus efectos adversos.
El curso de tratamiento recomendado con esketamina (Spravato®) consiste en la administración por inhalación dos veces por semana, durante 4 semanas, con dosis de refuerzo (técnicamente: «dosis de rescate») si no se consigue un control adecuado. El tratamiento con esketamina se debe asociar a un tratamiento de base con alguno de los clásicos antidepresivos por vía oral.
Dadas las especiales circunstancias de este tratamiento, se ha de administrar en un entorno hospitalario, supervisando al paciente durante las siguientes dos horas. Se contraindica que se conduzca o maneje maquinaria peligrosa durante el día de tratamiento.
La esketamina (S-ketamina), como la ketamina (mezcla racémica de los dos estereoisómeros, S y R), tiene potencial de abuso, pudiendo desencadenar episodios psicóticos.
En principio, el coste de un mes de tratamiento con esketamina oscilará entre 4.720 y 6.875 dólares ($4,720 y $6,785). La facturación global de medicamentos antidepresivos supera los doce mil millones de dólares. Hasta la aprobación de Spravato® (esketamina), prácticamente todos los antidepresivos se comercializan en versiones genéricas.
Los antidepresivos más prescritos hoy día son los «inhibidores de la recaptación de serotonina» o los «inhibidores mixtos de recaptación de serotonina y noradrenalina». Todos ellos tienen un período de latencia de 3 o 4 semanas antes de que sus efectos terapéuticos se hagan manifiestos. Su eficacia resolutiva es limitada, siendo preciso recurrir en los casos graves a los antidepresivos más antiguos (tricíclicos), más eficaces pero mucho más yatrogénicos.
En este contexto, la esketamina puede suponer una verdadera novedad. Por su inmediatez de acción se podría comparar con la terapia electroconvulsiva (electroshock) pero realizada mediante la inhalación de un fármaco durante un tiempo limitado (4 semanas).
Durante la evaluación clínica de la esketamina, se ha identificado un metabolito que podría ser útil como medicamento antidepresivo.
En los ensayos clínicos realizados, financiados por el laboratorio comercializador, Janssen Pharmaceuticals Inc., los pacientes se distribuyeron de manera aleatoria y con doble-ocultación («doble-ciego»), en dos grupos, tratados respectivamente con esketamina («grupo de estudio») o placebo («grupo placebo»). Durante un estudio de 1 mes (duración de un ciclo de tratamiento con esketamina), los pacientes del «grupo de estudio» redujeron su puntuación en las escalas de valoración de la enfermedad depresiva en 21 puntos, y los del «grupo placebo» solo en 17.
Sin embargo, en otro estudio, también financiado por Janssen Pharmaceuticals, Inc., las diferencias entre los grupos «de estudio» y «placebo» no fueron estadísticamente significativas.
Como criterio general, antes de aprobar un nuevo medicamento la Food and Drug Administration (FDA) suele exigir resultados favorables en al menos dos ensayos clínicos a corto plazo. Sin embargo, la FDA ha sido menos exigente en el caso de la esketamina, aceptando como criterio el índice de recaídas en personas que respondieron de manera favorable a un primer ciclo de tratamiento. En este sentido, Janssen Pharmaceuticals Inc., notificó un índice de recaída del 25% tras un ciclo de tratamiento, en relación con un 45% en el grupo que recibió spray placebo. Todos los participantes del ensayo tenían diagnóstico confirmativo de depresión refractaria a tratamientos convencionales.
Una de las cuestiones no resuelta es si la esketamina inhalada tiene ventajas objetivas en relación a la ketamina intravenosa.
Glen Brooks, fundador y director médico del New York Ketamine Infusions, una clínica privada de Manhattan, New York declaró haber tratado a más de 2.300 personas de todas las edades con infusiones intravenosas de ketamina, bajo diagnósticos tan variados como «síndrome de estrés postraumático», ansiedad generalizada, trastorno obsesivo-compulsivo, y depresión.
Las experiencias no regladas con la administración de infusiones intravenosas de ketamina indican que las respuestas son más favorables en adolescentes y adultos jóvenes que en personas de edad avanzada Esta observación es concordante con la información suministrada por Janssen Pharmaceuticals, según la que, a partir de 65 años, la eficacia de la esketamina no es significativamente superior a la observada con placebo.
 La ketamina se desarrolló hace más de medio siglo como una alternativa más segura a la fenciclidina (también conocida como PCP). La ketamina se ha utilizado en entornos tan diversos como los quirófanos hospitalarios, los campos de batalla y las clínicas pediátricas. Durante la anestesia con ketamina el paciente permanece con los ojos abiertos. Parece actuar «desconectando» las regiones medias del cerebro (hipocampo, tálamo, hipotálamo) con las superiores (corteza cerebral). Desde el año 1985, la ketamina se halla incluida en el listado de medicamentos esenciales de la Organización Mundial de la Salud.
La ketamina se desarrolló hace más de medio siglo como una alternativa más segura a la fenciclidina (también conocida como PCP). La ketamina se ha utilizado en entornos tan diversos como los quirófanos hospitalarios, los campos de batalla y las clínicas pediátricas. Durante la anestesia con ketamina el paciente permanece con los ojos abiertos. Parece actuar «desconectando» las regiones medias del cerebro (hipocampo, tálamo, hipotálamo) con las superiores (corteza cerebral). Desde el año 1985, la ketamina se halla incluida en el listado de medicamentos esenciales de la Organización Mundial de la Salud.
A partir de la década de 1990, surgió el interés por la ketamina como potencial fármaco antidepresivo, cuando Phil Skolnick modelizó que la intervención sobre las vías neuronales glutaminérgicas (excitadoras) podría relacionarse con efectos antidepresivos.
En el año 2000, el grupo de trabajo de Robert M. Berman del Connecticus Mental Health Center y de la Yale University comunicó que dosis subanestésicas de ketamina daban lugar a un rápido alivio de las depresiones.
En el año 2006, Carlos Zarate Jr de los National Institute of Mental Health publicó que 18 personas con depresión refractaria mejoraron de manera notoria a las pocas horas de recibir una infusión intravenosa de ketamina.
Sorprende que la eficacia de la ketamina no se limite a depresión, abarcando también otras alteraciones del estado de ánimo, como la ansiedad grave y la anhedonia. Se podría hallar así justificación de los extensos usos delas infusiones intravenosas de ketamina en algunas clínicas privadas.
Uno de los aspectos más valiosos de la esketamina es la evitación de ideaciones suicidas en pacientes con depresiones muy graves.
No se sabe si la rápida acción antidepresiva está directamente relacionada con los cuadros psicóticos, incluido la percepción extracorpórea.
Zaragoza, a 9 de marzo de 2019
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Florentino Ballesteros, 11-13
50002 Zaragoza

