Nuestros enemigos del submundo de lo visible, los microorganismos patógenos, que años atrás creíamos haber domeñado, están adquiriendo resistencias contra la mayoría de los antibióticos disponibles. A este problema se añade la paralización de la investigación de antibióticos verdaderamente novedosos.
Un efecto colateral es la quiebra económica de varias empresas que apostaron por la investigación antibiótica. Esta situación podría ser responsable de la muerte de más de diez millones de personas durante las próximas décadas.
Empresas como Achaogen y Aradigm han quebrado durante 2019. Algunas, con solvencia financiera, tales como Novartis y Allergan, han abandonado las líneas de investigación sobre nuevos antibióticos.
Otras empresas en las que se pusieron grandes esperanzas, tales como la norteamericana Melinta Therapeutics han informado a sus accionistas de una preocupante falta de liquidez.
La perspectiva del desarrollo de nuevos antibióticos, tanto desde un punto de vista científico como económico, es muy sombría. La situación apenas ha trascendido a los medios de comunicación. La sociedad cree estar protegida por la disponibilidad de suficientes moléculas antibióticas, pero no es consciente que cada vez es más común contraer infecciones, sobre todo hospitalarias, que nos retrotraen a la era pre-antibiótica.
Las inversiones para el descubrimiento de antibióticos verdaderamente novedosos son enormes. Por otra parte, cuando se consigue un nuevo antibiótico, su empleo durante unos pocos días, unido a las restricciones de prescripción para prevenir la aparición de cepas resistentes, limita el tiempo de venta en exclusividad antes de la aparición de marcas genéricas. En estas circunstancias, los laboratorios prefieren dirigir sus inversiones a medicamentos que se usarán durante años (a veces durante toda la vida) y sobre los que los Organismos Reguladores no impondrán cortapisas para su libre prescripción.
Además, la morbilidad y mortalidad debida a infecciones resistentes a todos los antibióticos y quimioterapéuticos conocidos está aumentando en todo el mundo. Si la situación no cambia drásticamente en los próximos años, y nada induce a pensar que vaya a ser así, la Organización Mundial de la Salud, anticipa una mortandad por infecciones multirresistentes de más de diez millones de personas a mediados del siglo actual.
Los nuevos antibióticos han demostrado ser eficaces para combatir de manera resolutiva algunos de los gérmenes más aviesos, como los causantes del ántrax, las neumonías bacterianas y las infecciones por Escherichia coli. El panorama se tornó menos esperanzador tiempo ha.
 La experiencia de la empresa biotecnológica Achaogen es paradigmática. Tras tres lustros de trabajo y millones de dólares invertidos, consiguió la autorización (junio 2018) por la Food and Drug Administration (FDA) estadounidense de Zemdri® (Plazomicin), un aminoglucósido para el tratamiento de las infecciones complicadas del tracto urinario. En julio de 2019 la Organización Mundial de la Salud añadió Zemdri® a la lista de «medicamentos esenciales». Aun cuando esta decisión puede parecer un éxito, la consideración de «esencial» restringe su prescripción, reduciendo el retorno de la inversión.
La experiencia de la empresa biotecnológica Achaogen es paradigmática. Tras tres lustros de trabajo y millones de dólares invertidos, consiguió la autorización (junio 2018) por la Food and Drug Administration (FDA) estadounidense de Zemdri® (Plazomicin), un aminoglucósido para el tratamiento de las infecciones complicadas del tracto urinario. En julio de 2019 la Organización Mundial de la Salud añadió Zemdri® a la lista de «medicamentos esenciales». Aun cuando esta decisión puede parecer un éxito, la consideración de «esencial» restringe su prescripción, reduciendo el retorno de la inversión.
La primavera pasada (2019) el valor de las acciones de la compañía, Achaogen, era prácticamente cero. La empresa no consiguió la financiación necesaria para llevar a cabo los ensayos clínicos adicionales exigidos por la US-FDA. La empresa se vio obligada a despedir a sus científicos, vender su tecnología y declararse en quiebra.
Aun cuando existe consenso acerca de la necesidad de implementar medidas que favorezcan las inversiones en el área de la investigación antibiótica, todas las propuestas parecen languidecer cuando se trata de llevarlas más allá de las palabras. Las inversiones en investigación antibiótica se han convertido en capital de riesgo, cada vez más rechazado por los accionistas de las empresas farmacéuticas. La incertidumbre es muy elevada y los beneficios, si se logran, son cada vez más escasos. Hacen falta, pues, incentivos suficientes para dinamizar la investigación.
La industria farmacéutica confronta otro desafío: tras años de advertencias contra la prescripción indiscriminada de antibióticos, muchos médicos son reacios a recetar los antibióticos más novedosos, limitando la capacidad de las empresas farmacéuticas para obtener beneficio de la inversión realizada. En este escenario, la prescripción preferente de marcas genéricas de antibióticos más antiguos frente las nuevas moléculas crea un sesgo desfavorable a la innovación.
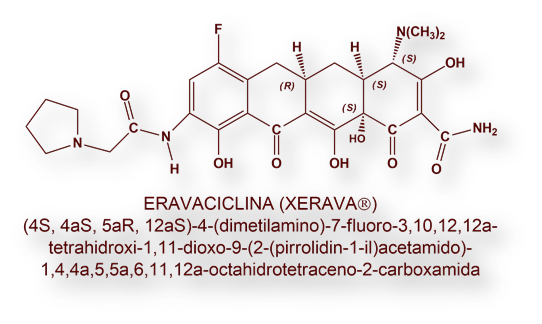 Muchos de los nuevos antibióticos comercializados son caros, sobre todo en relación con los más antiguos vendidos de manera mayoritaria en versiones genéricas. Por ejemplo, un ciclo de tratamiento con Xerava® (Eravaciclina), del laboratorio Tetraphase Pharmaceuticals, puede costar alrededor de dos mil dólares ($2,000). Sin embargo, mientras muchos medicamentos anticancerosos de elevado precio apenas incrementan la supervivencia de un enfermo terminal varios meses, un antibiótico puede curar a un enfermo de manera resolutiva.
Muchos de los nuevos antibióticos comercializados son caros, sobre todo en relación con los más antiguos vendidos de manera mayoritaria en versiones genéricas. Por ejemplo, un ciclo de tratamiento con Xerava® (Eravaciclina), del laboratorio Tetraphase Pharmaceuticals, puede costar alrededor de dos mil dólares ($2,000). Sin embargo, mientras muchos medicamentos anticancerosos de elevado precio apenas incrementan la supervivencia de un enfermo terminal varios meses, un antibiótico puede curar a un enfermo de manera resolutiva.
Desde el descubrimiento hasta la comercialización de Xerava® transcurrió alrededor de una década a pesar de que Eravaciclina resolvía un problema médico urgente: las infecciones multirresistentes, definidas como MRSA (Meticilin Resistent Staphylococcus aureus) y CRE (Carbapenem Resistant Enterobacteriaceae). Las infecciones causadas por este tipo de bacterias causan la muerte a miles de personas cada año.
Este retraso de la autorización de Xerava® hizo caer el valor de las acciones del laboratorio (Tetraphase Pharmaceuticals) desde los $40 hace un año a $2 en la actualidad (2020). Como consecuencia se despidió a 40 científicos y, lo que es peor, se interrumpieron las investigaciones de otros tres potenciales antibióticos que se hallaban en lo que en la jerga se denomina pill-line.
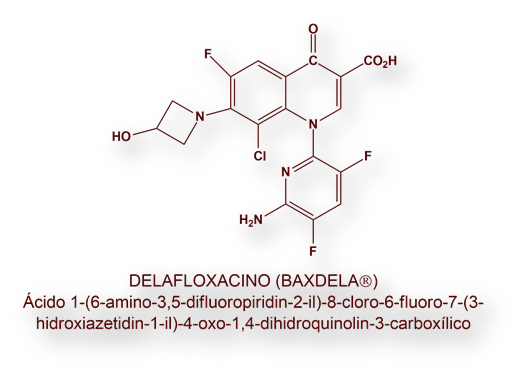 Para Melinta Therapeutics el futuro es también sombrío. El valor nominal de sus acciones ha caído un 45%. El laboratorio fabrica cuatro antibióticos, entre ellos Baxdela® (Delafloxacino), una quinolona antibiótica aprobado recientemente por la Food and Drug Administration (FDA) estadounidense para las neumonías comunitarias complejas que precisan hospitalización. Debido a la viabilidad comprometida de Melinta Therapeutics también lo está la investigación de Baxdela®
Para Melinta Therapeutics el futuro es también sombrío. El valor nominal de sus acciones ha caído un 45%. El laboratorio fabrica cuatro antibióticos, entre ellos Baxdela® (Delafloxacino), una quinolona antibiótica aprobado recientemente por la Food and Drug Administration (FDA) estadounidense para las neumonías comunitarias complejas que precisan hospitalización. Debido a la viabilidad comprometida de Melinta Therapeutics también lo está la investigación de Baxdela®
Desarrollar nuevos antibióticos no es una tarea sencilla; aún menos hallar una nueva clase de antibióticos. Solo han surgido dos familias durante los últimos veinte años; los demás antibióticos comercializados son simples modificaciones (me too) de otros ya existentes.
Mientras en la década de 1980 había dieciocho empresas farmacéuticas involucradas en investigación antibiótica, hoy día (2020) solo hay tres.
Diversos organismos filantrópicos, tales como Global Antibiotic Research and Development Partnership, han dejado constancia de su creciente inquietud sobre el asunto.
La inversión asociada al desarrollo de una molécula antibiótica supera los 2,6 millones de dólares. Algunas empresas involucradas en la investigación antibiótica sugieren que se las catalogue como un bien de carácter global. Ello implicaría incentivar la investigación mediante exenciones tributarias, prórroga de los derechos de patente, y su almacenaje estratégico frente a crisis potenciales.
Un proyecto de ley (DISARM Act propugna que Medicare reembolse a los hospitales los costes de los tratamientos con antibióticos novedosos de valor crítico.
Durante la pasada década BARDA (Biomedical Advanced Research and Development Authority) ha llevado a cabo un programa con el que se pretende desarrollar nuevos y valiosos fármacos antimicrobianos, si bien con la última finalidad de afrontar potenciales crisis sanitarias de origen bélico o terrorista. Un aspecto incidental, pero no menor, de dicho programa es el problema de la resistencia.
Achaogen y sus trescientos trabajadores mantuvieron la esperanza de que la intervención gubernamental hiciese viable la empresa, sobre todo tras obtener 124 millones de dólares de BARDA con la que desarrollaron el antibiótico Zemdri® (Plazomicina). Hace tres años (2017) Achaogen tenía una capitalización de mil millones de dólares, y Zemdri® fue autorizado por la Food and Drug Administration (FDA) estadounidense bajo la consideración de Breakthroug Therapy (una de las estrategias de aprobación acelerada de medicamentos de especial interés). Contra toda previsión, el laboratorio entró en un rápido proceso de descapitalización. En junio de 2019 vendió a Cipla USA (división estadounidense del laboratorio indio) los derechos de comercialización de Zemdri® por 16 millones de dólares (un cifra ridículamente baja) y despidió a sus investigadores. La mayoría se han integrado en proyectos de investigación más seguros, tales como la oncología.
Existe una creciente preocupación, pero no se están tomando medidas. La urgencia no solo procede de la falta de anuencia en las decisiones, sino en el tiempo que transcurrirá desde que éstas se adopten hasta la plasmación de soluciones efectivas.
Zaragoza, a 9 de enero de 2020
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Florentino Ballesteros, 11-13
50002 Zaragoza