Nombre IUPAQ del Molnupiravir (EIDD-2801):
[(2R, 3S, 4R, 5R)-3,4-dihidroxi-5-[4-(hidroxioxamino)-2-oxopirimidin-1-il] oxolan-2-il] metil-2-metilpropanoato
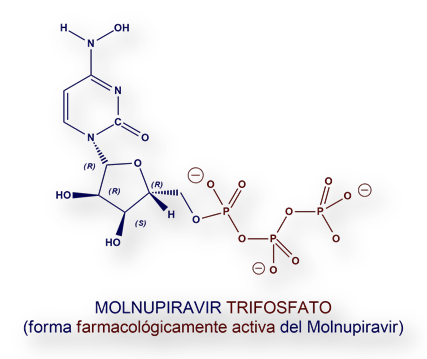 EIDD-2801 (Molnupiravir) es el isopropiléster, pro-fármaco de [N-(4)-hidroxicitidina, también designado EIID-1931.
EIDD-2801 (Molnupiravir) es el isopropiléster, pro-fármaco de [N-(4)-hidroxicitidina, también designado EIID-1931.
EIDD-2801se hidroliza in vivo, distribuyéndose en tejidos a la forma activa 5’-trifosfato. Molnupiravir-trifosfato se incorpora en el ARN de los virus (reacción catalizada por una polimerasa vírica), dando lugar a «mutación catastrófica» (así se denomina) para el virus. Estudios recientes han mostrado que EIDD-2801 (Molnupiravir) inhibe la replicación de los coronavirus, incluyendo el SARS-CoV-2 (responsable del Covid-19). Estos efectos se han observado tanto in vivo (en ratones) como in vitro (cultivos de células epiteliales bronquiales).
 N (4)-hidroxicitidina (EIDD-1931) es un análogo ribonucléosido de la citosina que induce mutaciones en los viriones ARN. Su primera descripción en la literatura científica data de 1830, donde se daba cuenta de su potencial para inducir mutaciones en bacterias y fagos (virus que destruyen bacterias). Inicialmente se demostró su actividad antiviral contra el virus de la encefalitis equina venezolana y el coronavirus HCoV-NL63 in vitro, un tipo de coronavirus responsable de resfriados comunes. Se ha usado como virucida por su acción mutagénica frente a coronavirus de quirópteros (estudios en ratones). Su forma farmacológicamente activa es el trifosfato de N (4)-hidroxicitidina. La imposibilidad de lograr patentar este producto (dada su antigüedad) ha estimulado la síntesis de análogos, uno de ellos es Molnupiravir (EIDD-2801), registrado por Merck, que ha decidido eximir su fármaco de los derechos de patente en 105 países con bajos estándares de desarrollo socioeconómico. Ello puede ser de gran ayuda en muchas regiones del mundo con importantes limitaciones para acceder a la vacunación anti-covid-19.
N (4)-hidroxicitidina (EIDD-1931) es un análogo ribonucléosido de la citosina que induce mutaciones en los viriones ARN. Su primera descripción en la literatura científica data de 1830, donde se daba cuenta de su potencial para inducir mutaciones en bacterias y fagos (virus que destruyen bacterias). Inicialmente se demostró su actividad antiviral contra el virus de la encefalitis equina venezolana y el coronavirus HCoV-NL63 in vitro, un tipo de coronavirus responsable de resfriados comunes. Se ha usado como virucida por su acción mutagénica frente a coronavirus de quirópteros (estudios en ratones). Su forma farmacológicamente activa es el trifosfato de N (4)-hidroxicitidina. La imposibilidad de lograr patentar este producto (dada su antigüedad) ha estimulado la síntesis de análogos, uno de ellos es Molnupiravir (EIDD-2801), registrado por Merck, que ha decidido eximir su fármaco de los derechos de patente en 105 países con bajos estándares de desarrollo socioeconómico. Ello puede ser de gran ayuda en muchas regiones del mundo con importantes limitaciones para acceder a la vacunación anti-covid-19.
El acuerdo con Medicines Patent Pool, organización que trabaja para hacer accesibles las medicinas y la tecnología médica a países pobres, permitirá a empresas farmacéuticas de esos 105 países fabricar Molnupiravir sin verse obligadas a pagar regalías a Merck.
Dos estudios clínicos combinados (fases 2/3) financiados por Merck mostraron que la toma de Molnupiravir por personas infectadas por covid-19 redujo a la mitad el número de hospitalizaciones y fallecimientos. En base a estos resultados, algunas naciones establecieron acuerdos para la adquisición de importantes stocks del fármaco, aun antes de su autorización por las autoridades reguladoras.
Se espera que los fabricantes de medicamentos genéricos en los países en desarrollo comercialicen Molnupiravir por $20 por tratamiento (5 días). El mismo tratamiento en Estados Unidos prevé un coste de $712.
Según Knowledge Ecology International (organización sin ánimo de lucro) el acuerdo es importante porque afecta a más de la mitad de la población mundial.
Merck ya había otorgado licencias de fabricación de Molnupiravir a ocho fabricantes indios de medicamentos genéricos. Sin embargo, limitar la producción en uno solo entrañaba riesgos, tanto técnicos como políticos. Por ello se plantea diversificar la fabricación siempre y cuando se cumplan los requerimientos de la Organización Mundial de la Salud. Merck ha declarado que transferirá tecnología a laboratorios de esos países para que puedan producirlo siguiendo las GMP (Good Manufacturing Proceeding). La actitud de Merck choca frontalmente con Pfizer y Moderna Therapeutics, quienes se negaron a la transferencia de tecnología de ARN mensajero a países de África, Centroamérica, Sudamérica y Asia para la producción local de sus vacunas anti-covid-19.
Cuando se ultima este artículo (4 de noviembre de 2021), Reino Unido, seguido horas después por la European Medicine Agency, han autorizado Molnupiravir, registrado como Lagevrio®.
El año pasado (2020) el gobierno federal estadounidense adquirió gran parte de la producción de Remdesivir tras la demostración de que podía acelerar la recuperación de pacientes con covid-19. Actualmente mantiene una estrategia similar en relación con Molnupiravir. El acuerdo de adquisición de 1,7 millones de tratamientos (dosis para 5 días) al coste de 1,2 mil millones de dólares está condicionado a que la Food and Drug Administration emita un informe favorable a la autorización del fármaco. Tal cantidad representa aproximadamente el 20% de la capacidad de producción de la compañía farmacéutica.
Otras naciones (Australia, Nueva Zelanda y Corea del Sur) han firmado con Merck acuerdos similares.
Con su actual decisión, Merck trata de resarcir la pésima imagen de hace alrededor de dos décadas cuando vendió sus medicamentos contra el VIH a países africanos a precios inasumibles para estas empobrecidas naciones.
La administración oral de Molnupiravir lo hace muy adecuado para su empleo en sistemas sanitarios precarios con difícil acceso a dispensarios y otros centros sanitarios. Una ventaja adicional es que no precisa conservación en frío. Hasta la aparición de este fármaco (y posiblemente otro similar desarrollado por Pfizer) el tratamiento del covid-19 se fundamentaba en anticuerpos monoclonales.
Algunas empresas farmacéuticas indias a las que se concede licencia para fabricar el medicamento han declarado la posibilidad de producirlo a menos de $10 por tratamiento (5 días).
Durante la larga lucha por hacer accesibles los antirretrovirales (contra el VIH) a principios del presente siglo, Merck fue diana de numerosas y agrias críticas, que trata de expiar con su decisión actual.
En la actualidad, más de 50 empresas de todo el mundo tratan de obtener una subcontrata para fabricar sus versiones de Molnupiravir.
Pfizer también tiene en estadios finales de desarrollo un medicamento antiviral contra el covid-19.
Molnupiravir se desarrolló conjuntamente por Merck y Ridgeback Biotherapeutics, con sede en Miami, Estados Unidos, a partir de una molécula estudiada por primera vez en la universidad de Emory, Atlanta.
Merck ha solicitado a la Food and Drug Administration la autorización acelerada de Molnupiravir , de tal manera que la decisión de la Agencia podría producirse a principios de diciembre (2021). Las versiones fabricadas en terceros países deberán solicitar la aprobación a sus autoridades reguladoras. Para soslayar los procedimientos burocráticos, muchas empresas solicitarán la precalificación de la Organización Mundial de la Salud. Un ejemplo de este proceder es el seguido por Aspen Pharmacare, empresa sudafricana que prevé comercializar su versión de Molnupiravir a $20 por tratamiento de 5 días de duración.
Merck venderá Molnupiravir en países con rentas altas a un precio significativamente superior. Se pretende así que estos países financian el acceso del medicamento a 105 países con rentas bajas. Una situación similar se produjo con los medicamentos contra la malaria cuando Novartis AG., registró su preparado con dos nombres de fantasía, uno destinado a viajeros occidentales en países endémicos de paludismo, y otro, a precio casi de coste de producción, para los habitantes de estas regiones.
También existe el caso reciente del Sofosbuvir (Sovaldi®), un eficaz antiviral contra la hepatitis C. Mientras el coste del tratamiento es elevado en países occidentales, Gilead Sciences (laboratorio desarrollador) permitió su fabricación y comercializador a costes de producción en muchos países, sobre todo en Egipto, con la mayor prevalencia mundial de hepatitis C.
Sibongile Tshabalala, presidenta de Treatment Action Campaing, organización sudafricana que tanto pleiteó para hacer accesibles los tratamientos antirretrovirales frente a la codicia de las multinacionales farmacéuticas, considera un éxito, casi una expiación, la decisión de Merck con Molnuparivir. [Recuérdese que Sudáfrica tiene la mayor prevalencia mundial de infección por VIH y SIDA].
Los acuerdos de Merck excluyen a Rusia y la República Popular China, considerados de renta media; pero también a la mayoría de Centro y Sudamérica.
Zaragoza, a 5 de noviembre de 2021
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Zaragoza

