Los coronavirus humanos (HCoVs) se han considerado desde su descubrimiento en la década de 1960, unos virus inconsecuentes; pero, ¡ya ven!, no hay enemigos menores.
Hasta el siglo actual, los coronavirus solo eran responsables de entre el 10% y 30% de las infecciones de tracto respiratorio superior (los resfriados comunes). Son ARN virus, clasificados en cuatro géneros: α, β, ꝩ, δ. Solo los géneros α y β son infecciosos para los humanos. Las cuatro cepas que causan las infecciones del tracto respiratorio superior en humanos (HCoV 229E, NL63, OC43, HKU1) son endémicas en todo el mundo. Los principales reservorios animales para estos coronavirus son los murciélagos. Otros animales, tanto salvajes como domésticos, actúan como hospedadores intermediarios contagiándose tras la mordedura de estos quirópteros. Durante el trasiego entre distintas especies se suelen producir mutaciones del genoma vírico, modificándose su capacidad infecciosa y su virulencia.
Las glucoproteínas (vistas al microscopio electrónico como agujas que sobresalen de la superficie más o menos esférica del coronavirus, de ahí su denominación) son críticas para la infección de las células (recuérdese que todos los virus son parásitos intracelulares).
Hasta el año 2002, los coronavirus recibieron escasa atención médica. En ese año, se describieron en la provincia china de Guangdong varios casos de una neumonía atípica. La peculiar neumonía adquirió entidad epidémica afectando a más de veinte países. La nueva enfermedad se designó con el acrónimo SARS (Severe Acute Respiratory Syndrome) y al germen causal β-HCoV que, a partir de entonces, se denominó SARS-CoV. Los primeros humanos se infectaron en mercadillos callejeros donde se manipulaban animales vivos, en este caso civetas y mapaches. Sin embargo, pronto se tomó conciencia que estos animales eran segundos hospedadores del virus, siendo los murciélagos sus reservorios naturales. La sintomatología del SARS se limitaba a fiebre, tos, disnea (insuficiencia respiratoria) y, más raramente, diarrea acuosa. Entre el 20 y el 30% de los infectados precisaba ventilación mecánica; y aproximadamente el 10% de todos los infectados fallecían, de preferencia personas añosas y con otras patologías crónicas. Se notificaron algunos contagios directos entre humanos, pero se ceñían al ámbito hospitalario, donde se hallaban los enfermos más graves, posiblemente con una mayor «carga viral». Esta expansión nosocomial (es decir, en un contexto hospitalario) se explicó porque la glucoproteína-S del SARS-CoV se engarzaba a una enzima («angiotensina-convertasa») más abundante en las células bronquiales del tracto respiratorio inferior, no tanto en las vías respiratorias superiores. La distribución de esta enzima (predominante en el tracto respiratorio inferior) explicaba que el máximo de infección ocurriese al cabo de unos 10 días del contagio, cuando la mayoría de los pacientes ya habían sido hospitalizados. En no pocas situaciones era necesario intubar a los pacientes, técnica cruenta que contribuía indirectamente a la expansión nosocomial de la infección.
La internacionalización de la epidemia del SARS partió del hotel Metropole de Hong Kong. Otro brote se produjo en el enorme complejo de viviendas Amoy Gardens, donde se evidenció la transmisión directa entre humanos fuera del medio hospitalario. Hoy día se sigue ignorando el factor (o factores) que determinaron el salto de la transmisión zoonótica (de animal a humano) al contagio directo entre humanos. La improbabilidad (no imposibilidad) de contagio directo entre humanos hizo que la epidemia terminase de manera tan súbita como surgió, sin que se llegase a utilizar la vacuna que se desarrolló al cabo de 20 meses de iniciarse la epidemia. Se contagiaron 8.098 personas, de las que murieron 774 (algo menos de un 10%).
En el año 2012, otro β-Cov (β-coronavirus) se aisló del esputo de un hombre saudí que terminó falleciendo por fallo respiratorio. Fue el primer caso de otro síndrome neumónico, el denominado MERS (acrónimo en inglés de Middle East Respiratory Syndrome). Al coronavirus responsable se le designó MERS-CoV. A diferencia del SARS, este nuevo virus no se expandió mundialmente, quedando circunscrito a la península de Arabia y unos pocos países relativamente alejados, sobre todo Irán y Argelia. En este caso la transmisión era únicamente zoonótica, afectando a los cuidadores de camellos. No obstante se produjeron algunos contagios nosocomiales (hospitalarios), a partir de los denominados supertransmisores (personas con gran contagiosidad). Estos brotes hospitalarios llegaron a comprometer los sistemas de salud de algunos de los países afectados. La incidencia del brote alcanzó un máximo coincidiendo con la época de nacimiento de las crías de camello. Al parecer, los murciélagos (muy abundantes en los oasis del desierto) mordían a las crías de camellos, desde donde el virus contagiaba a los cuidadores. La infección por MERS-CoV afectó a 2.494 personas. Entre el 50 y el 89% de los infectados precisaron ventilación mecánica. La mortalidad fue del 36% de todos los infectados.
Los brotes de SARS y MERS compartían el hecho de ser neumonías atípicas graves (muy graves en el caso del MERS), pero también se observaban algunas diferencias significativas: la sintomatología gastrointestinal y el fallo renal agudo en los infectados por MERS, circunstancia que explicaría su elevada mortalidad. Al parecer la glucoproteína del β-MERS-Cov tiene afinidad por la enzima humana DPP4 («Dipeptidil-Peptidasa-4»), abundante en el tracto respiratorio inferior y en el gastrointestinal, así como en el riñón. [Obsérvese que algunos novedosos medicamentos antidiabéticos actúan mediante la inhibición de esta enzima].
Si bien el brote de MERS no causó la alarma mundial del SARS, a pesar de ser mucho más mortífero (36% MERS vs ~10% SARS), los dos brotes evidenciaron los riesgos asociados a las zoonosis virales, razón por la que la Organización Mundial de la Salud los incluyó desde el año 2017 en la lista de patógenos emergentes (Priority Pathogen List).
La decisión de la Organización Mundial de la Salud fue presciente: el 31 de diciembre de 2019, las autoridades de la República Popular China informaron de un brote de neumonía inusual en un mercado de pescado de la megalópolis de Wuhan, provincia de Hubei. Otro coronavirus era responsable de este nuevo brote neumónico; el número de infectados comenzó a incrementarse siguiendo una progresión geométrica (exponencial). En apenas 10 días un equipo de investigadores del Shanghai Public Health Clinical Center en colaboración con la Shool of Public Health descifró el genoma completo del virus. La entrega desinteresada de este logro científico posibilitó una respuesta global y rápida a esta infección emergente. Este nuevo coronavirus (Cov-19) tiene bastante homología [en su genoma] con el SARS. De hecho, ambos coronavirus interactúan con la enzima «angiotensina-convertasa». A diferencia del SARS, este coronavirus (Covid-19) se transmite fácilmente entre humanos, tanto por vía respiratoria como por fómites (objetos contaminados). La pandemia se ha generalizado más allá de su foco inicial en la ciudad de Wuhan, primero en otros países cercanos, y actualmente en Europa y, de manera por ahora más limitada, en el continente americano. De África apenas se dispone información fiable, más allá de Egipto por razones turísticas.
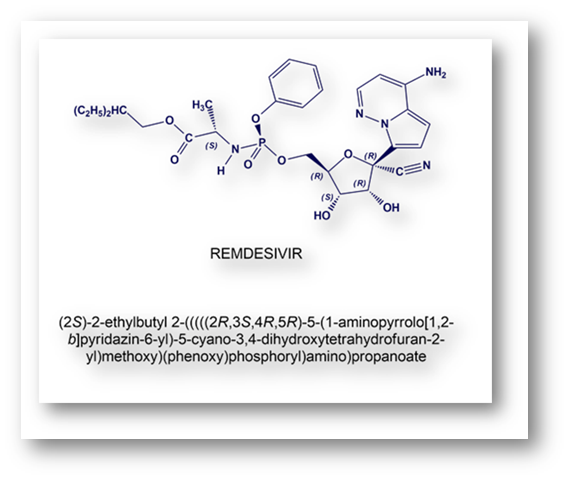
Algunos medicamentos se han ensayado para tratar a los infectados más graves: Remdesivir, bajo patente de Gilead Sciences (que ha entregado un importante número de dosis a la República Popular China). Este fármaco ya se utilizó durante la crisis del virus ébola en el año 2014.
Otros fármacos, los antirretrovirales Lopinavir, Ritonavir e Interferón-ꝩ se están empleando, sin que se hayan publicado los resultados.
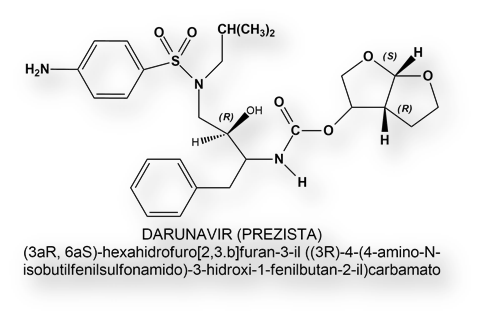
Así mismo, un medicamento antigripal, Umifenovir (Arbidol®), usado exclusivamente en Rusia y China, junto al antirretroviral Darunavir, se han probado, pero tampoco se han dado a conocer los resultados preliminares.
Otra alternativa es el desarrollo de una vacuna contra el Covid-19. Hasta hace algunos años el desarrollo de una nueva vacuna (bien con virus inactivados o atenuados) tardaba de 15 a 20 años. Así sucedió con las dos vacunas contra la polio: la inyectable de Jonas Salk que se formula con virus inactivados; y la oral de Albert Sabin, de empleo más general, que utiliza virus inactivados.
El surgimiento de virus emergentes con potencial pandémico ha obligado a reducir esta demora. La vacuna contra la pandemia del SARS del año 2003 se desarrolló en 20 meses; la vacuna contra la gripe A/Indonesia H5N1 del año 2006 se concluyó en 11 meses; la vacuna contra la gripe A/California H1N1 se logró en 4 meses; y la vacuna contra el virus Zika tardó solo 3,5 meses. Cabe prever, pues, que la vacuna contra Covid-19 no se demore demasiado. Sin embargo, el talón de Aquiles de estos procedimientos acelerados de elaboración y autorización, es la falta de estudios de seguridad a largo plazo.
Los coronavirus no son los únicos virus emergentes. Otros menos conocidos, como Nipah, Hendra, Menangle o Marburg (por mencionar los menos conocidos) han causado brotes muy limitados que no han trascendido del ámbito local En estos virus, sus reservorios son también los murciélagos.
En cuanto al Covid-19, el coronavirus que acapara la actualidad mundial, se desconoce cómo evolucionará durante las próximas semanas (este artículo se redacta el 13 de marzo de 2020). Mientras escribo este texto, la Organización Mundial de la Salud ha declarado pandemia a la infección por Covid-19. En cualquier caso terminará por desaparecer u ocultarse siguiendo la secuencia temporal de cualquier brote epidémico. Sin embargo, hemos de asumir que nuevos virus desencadenarán nuevas epidemias (o pandemias) en el futuro. Las enseñanzas que extraigamos de la actual crisis, más allá de atrabiliarios comportamientos sociales y políticos, deberían ser de gran utilidad para afrontar los riesgos del ignorado (y tantas veces menospreciado) submundo de lo visible.
Zaragoza, a 13 de marzo de 2020
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Florentino Ballesteros, 11-13
50002 Zaragoza