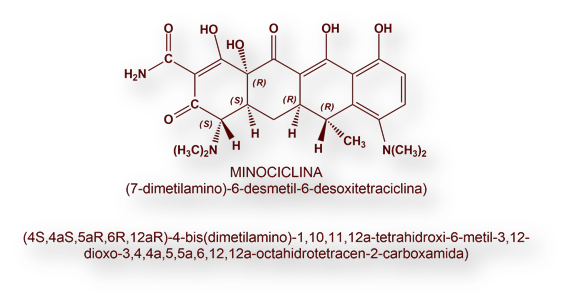
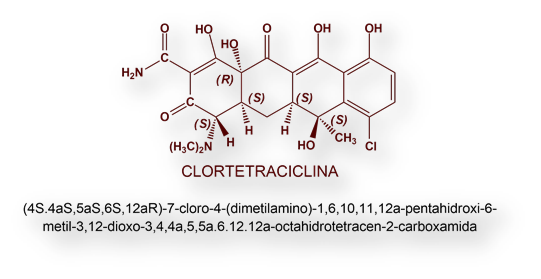
 En el verano de 1945 se recibió en los entonces laboratorios Lederle, en Pearl River, New York, una muestra de suelo conteniendo un actinomiceto dorado (Streptomyces aureofaciens) del que se aisló una molécula antibiótica a la que se denominó Clortetraciclina.
En el verano de 1945 se recibió en los entonces laboratorios Lederle, en Pearl River, New York, una muestra de suelo conteniendo un actinomiceto dorado (Streptomyces aureofaciens) del que se aisló una molécula antibiótica a la que se denominó Clortetraciclina.
Cuando se administraba por vía oral se comportaba como un antibiótico de amplio espectro con un patrón de susceptibilidades similar al del Cloranfenicol, pero sin efecto sobre la micobacteria tuberculosa.
A partir de 1948 se comenzó a producir en grandes tanques de fermentación a comercializándose como Aureomicina® de modo casi simultáneo al Cloranfenicol.
La comercialización de Clortetraciclina y Cloranfenicol amenazaba el entonces rentable negocio que Pfizer había conseguido con la Penicilina, cuyo precio, no obstante, se había reducido sustancialmente.
Como estrategia, Pfizer promovió un ambicioso proyecto de investigación en el que se estudiaron más de 100.000 muestras de suelo procedentes de los más diversos lugares del mundo en busca de potenciales nuevas moléculas antibióticas. De forma inesperada, la muestra de suelo que resultó óptima estaba ¡en los terrenos que rodeaban el edificio central del propio laboratorio! Allí se aislaron cepas de Streptomyces rimosus de las que obtuvo Oxitetraciclina, patentada en 1949, un año después de la Clortetraciclina.
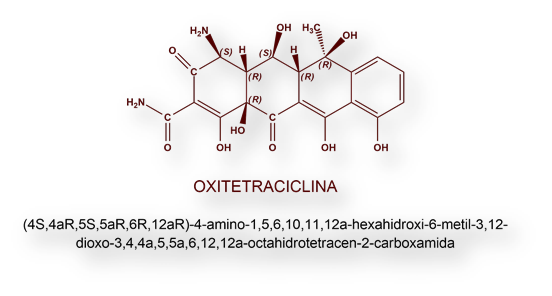 El grupo de Robert Woodward bajo el paraguas económico y científico de Pfizer dedujo en 1952 las estructuras químicas de ambos antibióticos, Clortetraciclina y Oxitetraciclina.
El grupo de Robert Woodward bajo el paraguas económico y científico de Pfizer dedujo en 1952 las estructuras químicas de ambos antibióticos, Clortetraciclina y Oxitetraciclina.
La Clortetraciclina tiene baja biodisponibilidad oral y su Vida Plasmática Media (T1/2) es breve, circunstancias que limitan su practicidad clínica en el tratamiento de infecciones sistémicas.
Hasta entonces Pfizer vendía los derechos de comercialización [de sus productos] a otros laboratorios. Al no disponer de suficiente red comercial, el laboratorio promocionó su más reciente antibiótico (Oxitetraciclina) en los medios de comunicación no-especializados. Durante los dos años siguientes gastó en publicidad el doble de lo invertido en descubrir la Oxitetraciclina (4 millones de dólares ¡de 1949!).
En 1952, como parte de una guerra científica y comercial, por el mercado farmacéutico antibiótico, Lederle y Bristol-Myers aislaron independientemente Tetraciclina a partir del actinomiceto del que Lederle había obtenido Clortetraciclina.
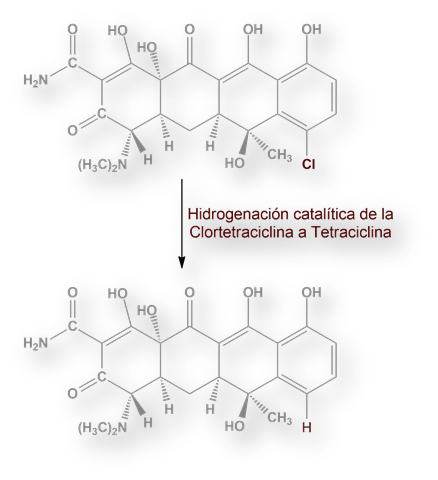 Casi simultáneamente Lloyd H.Conover de Pfizer obtuvo Tetraciclina mediante la hidrogenación catalítica de Clortetraciclina.
Casi simultáneamente Lloyd H.Conover de Pfizer obtuvo Tetraciclina mediante la hidrogenación catalítica de Clortetraciclina.
Los tres laboratorios involucrados en el desarrollo farmacéutico de las tetraciclinas (Lederle, Bristol-Myers, y Pfizer) reclamaron derechos de patente sobre el descubrimiento de la Tetraciclina. La patente se otorgó finalmente a Lloyd H. Conover, quien los vendió a empresas que deseaban desarrollar derivados semisintéticos. Su decisión fue demandada en base a la Ley anti-monopolio estadounidense (Sherman Antitrust Act[1], de 1890) con la que se trataba de evitar los monopolios y con ellos la fijación de precios al alza. Tras años de procesos judiciales, en 1982 el Tribunal de Apelación de Filadelfia dio la razón a Lloyd H. Conover. Pero, para entonces, las tetraciclinas habían perdido su aura de «antibióticos milagro», debido a la aparición de numerosas resistencias sobre todo por su empleo masivo en el ámbito hospitalario, así como en horticultura.
La promoción que Pfizer había llevado a cabo surtió efecto; los tres antibióticos (Tetraciclina, Clortetraciclina y Oxitetraciclina) se catalogaron de «antibióticos excepcionales». Se exageraban sus ventajas en relación a la Penicilina, dado que se podían administrar por vía oral (la primera formulación oral de Penicilina no se desarrolló hasta mediados de la década de 1950), pero la biodisponibilidad por vía oral era escasa, y alteraban la microbiota intestinal.
No obstante, las tetraciclinas siguieron siendo medicamentos de elección para condiciones clínicas como tracoma, psitacosis, «enfermedad de Lyme», «Fiebre de las Montañas Rocosas», Fiebre Q, e infecciones por clamidias; así como frente a casi todas las cepas de Haemophilus influenzae.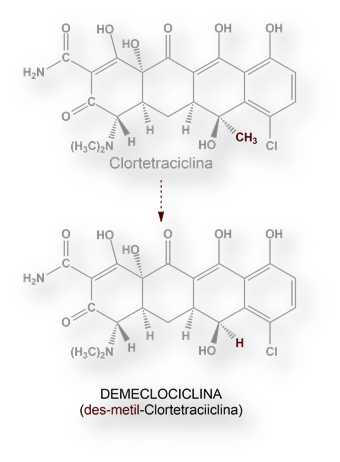
En el año 1957 laboratorios Lederle aisló Demeclociclina (desmetil-clortetraciclina) a partir de cepas mutantes Duggar de Streptomyces aureofaciens.
El aislamiento de Demeclociclina abrió la espita para la investigación y desarrollo de tetraciclinas semisintéticas.
Las tetraciclinas son moléculas muy poco hidrosolubles. Cuando se acidifica el medio para aumentar la solubilidad se produce la epimerización del sustituyente dimetilamino, lo cual disminuye notablemente la eficacia.
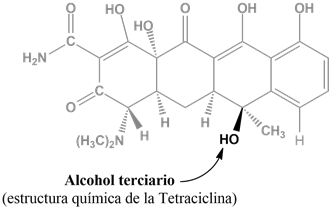
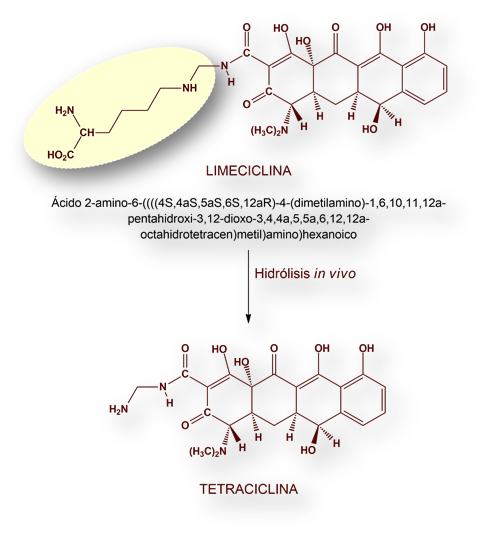
Otro problema es la eliminación catalítica del hidroxilo terciario. Su presencia determinaba que las formulaciones inyectables se tuvieran que inyectar inmediatamente tras la reconstitución del vial en agua estéril para inyección. El problema se soslayó mediante la reacción del grupo carboxamido con formaldehído y aminas para formar derivados hidrosolubles. De este modo se obtuvo Limeciclina, desarrollado en 1959 por Willy Logemann y Francesco Lauria, del Instituto Carlo Erba, Milán, Italia. Lymeciclina (tetraciclin-L-metilen-lisina) se formulaba en cápsulas orales que liberaban tetraciclina in vivo.
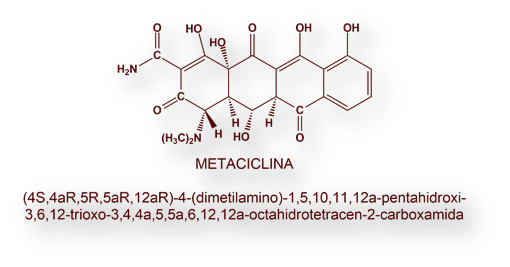
 Un año antes, en 1958, un grupo de trabajo de Pfizer eliminó el hidroxilo terciario de las tetraciclinas, mediante hidrogenolisis, proceso catalizado por carbón-paladio. La pérdida del hidroxilo terciario aumentaba tanto la estabilidad como la liposolubilidad. La molécula sintetizada se denominó Metaciclina (6-metilen-5-hidroxitetraciclina).
Un año antes, en 1958, un grupo de trabajo de Pfizer eliminó el hidroxilo terciario de las tetraciclinas, mediante hidrogenolisis, proceso catalizado por carbón-paladio. La pérdida del hidroxilo terciario aumentaba tanto la estabilidad como la liposolubilidad. La molécula sintetizada se denominó Metaciclina (6-metilen-5-hidroxitetraciclina).
A ésta le siguió la Doxiciclina (α-6-desoxitetraciclina), cuya características diferenciales más notorias fueron la mejor absorción intestinal y la reabsorción en los túbulos renales. El tiempo de permanencia del fármaco se incrementaba permitiendo una única dosis diaria.
De todas las tetraciclinas semisintéticas que siguieron a la Doxiciclina, la única que adquirió significación clínica fue la Minociclina (7-dimetilamino-6-desmetil-6-desoxitetraciclina), sintetizada en 1965 por Lederle Division de American Cyanamid. Su mayor lipofilia optimizaba su difusión tisular, incluso al sistema nervioso central, pero al precio de causar náusea, ataxia y vértigo. Se mostró eficaz en el tratamiento de las meningitis meningocócicas. Además, dado que se conseguían concentraciones significativas en lágrimas y saliva, se utilizó también para el tratamiento de los portadores del meningococo.
Mecanismo acción de las tetraciclinas.-
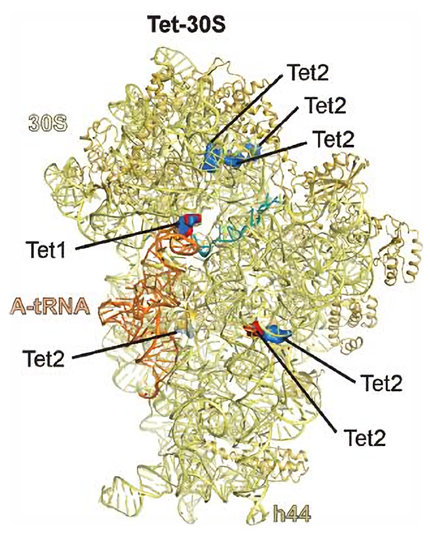 Modelo de la subunidad ribosómica 30S, con los lugares de unión de las tetraciclinas, siendo Tet1 y Tet2, las principales dianas farmacológicas.
Modelo de la subunidad ribosómica 30S, con los lugares de unión de las tetraciclinas, siendo Tet1 y Tet2, las principales dianas farmacológicas.
Las tetraciclinas antibióticas inhiben la síntesis proteica, mediante el bloqueo del engarce de aminoacil-ARNt al complejo ribosómico. Con ello se interrumpe el crecimiento (elongación) del ARNm y su traducción en proteínas.
Como mecanismo secundario, las tetraciclinas alteran la integridad de la membrana bacteriana permitiendo la exclusión de nucleótidos y otros compuestos fundamentales para el metabolismo celular.
La resistencia bacteriana a las tetraciclinas se debe a una menor acumulación del antibiótico en el interior de la bacteria. La resistencia está relacionada con la síntesis de determinadas proteínas de la membrana bacteriana codificadas por plásmidos (en bacterias Gram negativas). La resistencia bacteriana se puede transferir entre plásmidos mediante trasposones.
A concentraciones superiores a las terapéuticas, las tetraciclinas también inhiben la subunidad ribosómica 30S de las células de mamíferos.
Jawetz y Gunnison clasificaron en 1952 los fármacos quimioterapéuticos en bactericidas (Penicilina G) y bacteriostáticos (tetraciclinas). [Recomiendo la siguiente referencia bibliográfica: Jawetz E, Gunnison J B Studies on antibiotics synergism and antagonism: a scheme of combined antibiotic action. Antibiot. Chemother 1952; 2: 243].
Toxicidad de las tetraciclinas.-
Los efectos adversos de tipo gastrointestinal incluyen: náusea, dolor epigástrico, vómito y diarrea. Esta última [diarrea] se debe a la irritación directa del antibiótico no absorbido sobre la mucosa intestinal; y, en menor medida, por la alteración de la microbiota.
Se ha descrito esteatorrea debida a enterocolitis antibiótica o colitis pseudomembranosa. Este efecto adverso es más notorio en pacientes post-quirúrgicos. Las elevadas concentraciones que las tetraciclinas alcanzan en la bilis, facilitan la sobreinfección estafilocócica.
Las tetraciclinas administradas por vía oral están contraindicadas en pacientes con obstrucción intestinal. Se han de administrar con no menos de 100ml de agua, y, siempre que sea posible, con el paciente erguido.
Las reacciones anafilácticas son muy infrecuentes. Por otra parte, la reacción de Harris Herxheimer se ha observado cuando las tetraciclinas se prescriben para infecciones causadas por espiroquetas (tularemia, leptospirosis, brucelosis).
Las reacciones de foto-sensibilidad se ciñen exclusivamente al uso de Demeclociclina y, con mucha menor frecuencia, Doxiciclina.
El efecto más conocido es el riesgo de pigmentación de la dentición y otras estructuras óseas.
Todas las tetraciclinas se depositan en núcleos de calcificación activos de huesos y dientes. Este efecto adverso en la dentición, con implicación estrictamente cosmética, se descubrió cuando se administraban ciclos de tratamiento prolongados a niños con fibrosis quística. Es muy interesante la lectura de esta referencia bibliográfica: Shwachman H., et al. The effect on the a long-term antibiotic therapy in patients with cystic fibrosis of the pancreas. Antibiot. Annual 1969; 1958-1959, página 692.
La mineralización ósea tiene lugar desde la semana decimocuarta de la gestación (las tetraciclinas cruzan la barrera placentaria) hasta en recién nacido alcanza los dos o tres meses de vida, periodo de mayor riesgo de decoloración de la dentición; un segundo período de mineralización se produce desde los 4-5 meses de vida, hasta que el niño cumple 5 o 6 años. El riesgo de coloración dental (entre amarillenta y parduzca) es especialmente grave durante el primer año de vida debido a que la inmadurez renal impide el eficiente aclaramiento del antibiótico. De todas las tetraciclinas, Doxiciclina es la menos propensa a causarlo.
En cualquier caso, se CONTRAINDICA la prescripción de tetraciclinas a niños menores de 8 años. En Australia todas las preparaciones pediátricas de estos antibióticos se retiraron en 1977.
Toxicidad hepática.-
La toxicidad hepática se limita a las preparaciones intravenosas cuando la dosis total diaria excede 1 o 2g. La sintomatología incluye: náusea, vómito, fiebre, ictericia, hematemesis, fallo renal con acidosis e hipotensión. El cuadro puede derivar en coma irreversible.
Toxicidad renal.-
Las tetraciclinas se han vinculado con cinco tipos de daño renal, cuya descripción detallada trasciende el objeto de esta revisión. Son los siguientes:
- Agravamiento de un fallo renal preexistente.
- Toxicidad renal por esteatosis.
- Daño tubular renal.
- Diabetes insípida de causa renal causada por Demeclociclina.
- Nefritis intersticial.
Se han notificado otros efectos adversos (vestibulares, neurotóxicos) que por su particularismo trascienden en objetivo de esta revisión.
Bibliografía recomendada sobre las tetraciclinas:
- Chopra, I. Tetracycline antibiotics: mode of action, applications, molecular, and epidemiology of bacterial resistance. Microbiology and Molecular Biology Reviews 2001; 65(2): 232-26.
- Nguyen, F., et al. Tetracycline antibiotics and resistance mechanisms. Biological Chemistry 2014; 395(5): 559.
Zaragoza, a 23 de septiembre de 2020
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Zaragoza
[1] El senador por el Estado de Ohio promovió la Ley antimonopolio (Sherman Antitrust Act), que fue firmada por el Presidente en 1890, Benjamin Harrison.