Se han hecho públicas las conclusiones de un extenso estudio clínico en el que han participado más de 11.000 pacientes de 30 países sobre la eficacia (estimada en términos de disminución de la mortalidad) de Remdesivir en el tratamiento de covid-19. Los resultados, publicados online el 15 de octubre (2020), concluyen que no se observa una disminución de la mortalidad. Este estudio (Re-purposed antiviral drugs for COVID-19. Interim WHO SOLIDARITY trial result) ha sido financiado por la Organización Mundial de la Salud.
Sin embargo, existen discrepancias en la interpretación de los resultados. Proceden éstas de que el estudio se ha realizado en 30 países con diferentes protocolos de tratamiento, algunos inconsistentes, por lo que existen sesgos importantes que pueden desvirtuar la interpretación de los resultados.
Remdesivir se ensayó como tratamiento de la hepatitis C, y de la infección por el virus ébola.
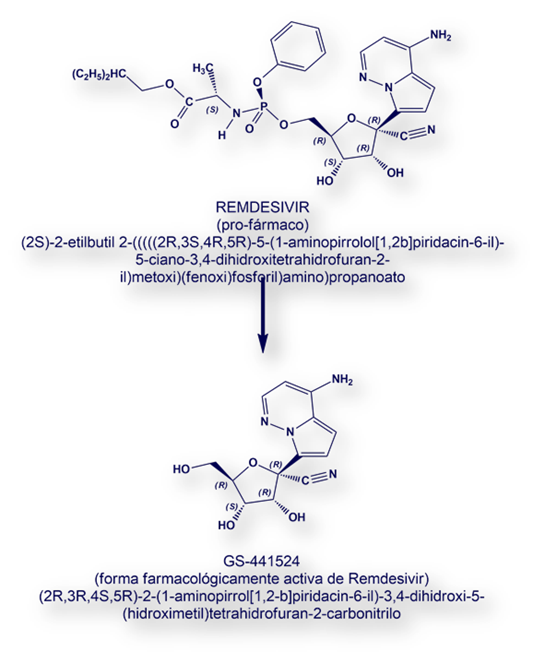
Redemsivir, un pro-fármaco (su forma farmacológicamente activa es GS-441524), se engarza con la enzima vírica RdRp (RNA-polimerasa RNA-dependiente) bloqueando la replicación vírica. Además, el fármaco (en su forma activa) se intercala en el ARN vírico bloqueando los mecanismos de corrección genética durante la replicación.
El laboratorio Gilead Sciences había sintetizado varias moléculas, además de Remdesivir, con este mecanismo de acción. Por razones nunca explicadas, el laboratorio abandonó esta línea de investigación.
Remdesivir ha resurgido del cajón de moléculas olvidadas. Cuando se estudió in vitro, Remdesivir se mostró eficaz contra todos los coronavirus estudiados. A este hecho siguieron esperanzadores resultados cuando se valoró en animales de experimentación.
Antes del verano (2020) muchos médicos comenzaron a prescribirlo a pacientes con covid-19 sin el aval de estudios clínicos rigurosos. El propio uso incrementó la demanda, y el laboratorio aprovechó esta circunstancia para entregar gratuitamente envases a médicos, quienes lo prescribían bajo criterio de «uso compasivo».
La Food and Drug Administration estadounidense (US-FDA) autorizó su empleo en pacientes con covid-19 el 1 de mayo (2020), tras un estudio auspiciado por los National Institutes of Health que mostró una modesta reducción del tiempo de recuperación en pacientes gravemente enfermos. Sin embargo, el estudio no evidenció una disminución objetiva de la mortalidad por covid-19.
Un análisis final publicado en la revista The New England Journal of Medicine el 8 de octubre (2020) sugirió una tendencia a la disminución de la mortalidad en determinados pacientes.
Tras conocerse los resultados del estudio auspiciado por la Organización Mundial de la Salud, cuestionando la reducción de mortalidad en pacientes con covid-19 tratados con Remdesivir, Gilead Sciences afirmó en una declaración que los resultados estaban sesgados por múltiples circunstancias; debido al propio diseño del estudio la heterogeneidad era significativa. ¿Se pueden dar por certeros los hallazgos obtenidos bajo estas condiciones?
El antiviral Remdesivir se ha convertido en una piedra angular del tratamiento del covid-19. Un ciclo de tratamiento en Estados Unidos tiene un coste de 3.120 dólares ($3,120). En España el coste es asumido íntegramente por el Sistema Nacional de Salud.
Remdesivir (Veklury®) se restringió en un principio para personas que estaban graves o muy graves (aquellas que precisaban oxigenoterapia o ventilación mecánica). A partir de agosto (2020) la autorización de uso se extendió a todos los pacientes hospitalizados, con independencia de su gravedad y surgieron preocupaciones por el abastecimiento.
El estudio de la Organización Mundial de la Salud, denominado SOLIDARITY incluyó a más de 11.300 adultos con covid-19 ingresados en 405 hospitales de 30 países. Los pacientes se distribuyeron de manera aleatoria en cuatro grupos, cada brazo de estudio tratado con medicamentos diferentes: Remdesivir, Hidroxicloroquina, Lopinavir (un antirretroviral), e interferón (o: interferón + Lopinavir). Alrededor de 4.100 pacientes no recibieron ningún fármaco, actuando como grupo placebo. No se detectó diferencia significativa entre los distintos grupos de tratamiento, y con el grupo placebo.
Un colofón del estudio es que ninguno de los medicamentos analizados (incluido Remdesivir) disminuye la mortalidad de los pacientes hospitalizados, los requerimientos de oxigenoterapia o ventilación mecánica, e incluso el tiempo de hospitalización.
Sin embargo, Remdesivir mantiene cierta llama de esperanza, al menos en los pacientes menos graves.
Se sabe que la forma más grave de covid-19 se debe, al menos en parte, a una desproporcionada respuesta inmune (la denominada «tormenta de citoquinas») que se manifiesta, aunque no siempre, al cabo de varios días del contagio. Bajo esta premisa, un tratamiento antiviral adecuado podría proteger al paciente del «fuego amigo» (su propio sistema inmune). Parece ser que la administración de Remdesivir más allá de este estadio tiene poco beneficio. El caballo ya se ha desbocado.
Zaragoza, a 17 de octubre de 2020
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Florentino Ballesteros, 11-13
50002 Zaragoza