El Cloranfenicol se aisló en 1947 (John Ehrlich y Quentin Bartz, de laboratorios Parke Davis) a partir de un actinomiceto[1] (una clase de hongo) obtenido de una muestra del suelo cerca de Caracas, Venezuela. A este actinomiceto se le denominó apropiadamente Streptomyces venezuelae. Cloranfenicol exhibió actividad antibiótica de amplio espectro y se mostró activo por vía oral[2], [3]
El primer uso del Cloranfenicol se produjo durante una epidemia de tifus exantemático que se extendió rápidamente por Bolivia. Más precisamente, en diciembre de 1947, se trataron a veintidós pacientes con rickettsiosis ingresados en el Hospital General de La Paz, capital administrativa, no política, de Bolivia, de los que cinco se hallaban extremadamente graves. Tras la administración del antibiótico todos los enfermos se recuperaron sin secuelas.
[El tifus exantemático es la denominación genérica para un grupo de infecciones bacterianas producidas por diversas especies del género Rickettsiae, si bien la especie Rickettsia prowazekii es la más común. Las rickettsias, son minúsculos bacilos, parásitos intracelulares, por lo que hay quien los clasifica entre las bacterias y los virus. Los piojos, garrapatas, pulgas y otros ácaros, actúan como vectores de transmisión. Rickettsia es patronímico de Howard Taylor Ricketts,].
Un grupo de trabajo de Parke Davis descifró la estructura química del Cloranfenicol, logrando la síntesis de laboratorio muy poco tiempo después[4].
El Cloranfenicol se convirtió en una verdadera mina de oro para el laboratorio Parke Davis que, gracias al antibiótico, entró en la élite de los laboratorios farmacéuticos mundiales. Más de ocho millones de pacientes fueron tratados con Cloranfenicol, hasta se comenzaron a publicar en diversas revistas médicas casos esporádicos de fallecimientos por aplasia de la médula ósea atribuible al Cloranfenicol. Se estimó una incidencia inicial de aplasia medular de 1:20.000 pacientes tratados, que más tarde se rebajó a 1:100.000. En la actualidad se acepta una prevalencia entre 1:10.000 y 1:45.000[5] [6]. El problema era que, si bien la incidencia del efecto adverso era muy baja, la mortalidad de los afectados era muy elevada (~80%). Tras una publicación en la revista Journal of the American Medical Association el 2 de agosto de 1952 de un caso clínico, el Organismo de Fármacos y Alimentos estadounidense (US-FDA) estudió la situación, permitiendo su comercialización pero con la exigencia al laboratorio comercializador, Parke Davis, de incluir en el material de acondicionamiento (el prospecto) la advertencia de «riesgo de aplasia medular durante su empleo continuado o frecuente».
PATOGÉNESIS DE LA APLASIA DE MÉDULA ÓESA POR CLORANFENICOL
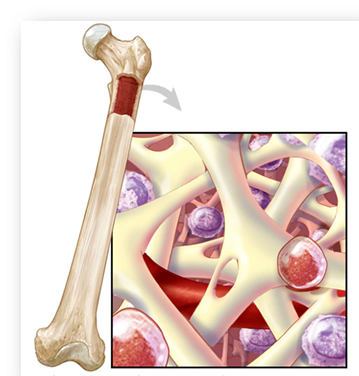 El riesgo de aplasia medular por Cloranfenicol no está relacionado con la duración de la terapia ni la dosis administrada. Se infiere, pues, una predisposición hereditaria. El principal problema es la imposibilidad de predecir la aparición de este grave efecto adverso, junto a la falta de modelos experimentales en animales para su estudio.
El riesgo de aplasia medular por Cloranfenicol no está relacionado con la duración de la terapia ni la dosis administrada. Se infiere, pues, una predisposición hereditaria. El principal problema es la imposibilidad de predecir la aparición de este grave efecto adverso, junto a la falta de modelos experimentales en animales para su estudio.
Cloranfenicol inhibe la duplicación del ADN, efecto más notorio en las células con una mayor tasa de duplicación, las precursoras de la línea hematopoyética. Tras varios estudios, se concluyó que el grupo «nitro» (‒NO2) en la estructura molecular del Cloranfenicol es responsable de la aplasia medular en personas con predisposición hereditaria, quienes metabolizan el grupo «nitro» a intermedios tóxicos para las células madre de la médula ósea. Ello explica que la molécula de Tianfenicol, en la que un grupo «metil-sulfonil» sustituye al grupo «nitro» del Cloranfenicol, no ha desencadenado casos de aplasia medular (véanse estructuras químicas al comienzo del artículo).
El Cloranfenicol y su análogo Tianfenicol, continúan siendo el tratamiento electivo en las salmonelosis, algunas meningitis bacterianas, así como en las rickettsiosis. También forma parte de preparaciones farmacéuticas para infecciones otológicas y oftalmológicas.
La sustitución del grupo «nitro» de Cloranfenicol por el grupo «metil-sulfonil» en el Tianfenicol determina que éste sea más hidrosoluble que aquél, no metabolizándose en el hígado (conjugación con ácido glucurónico). Tianfenicol se excreta casi íntegramente sin metabolizar, siendo necesario reajustar la dosis en caso de insuficiencia renal moderada a grave.
Cuando se redacta este artículo, solo Cloranfenicol está autorizado en España, formando parte de dos formulaciones, una para uso tópico (asociada a Hidrocortisona) indicada para dermatitis inespecíficas; y otra para uso oftalmológico en procesos inflamatorios de la conjuntiva (conjuntivitis) o los párpados (blefaritis).
Con independencia de lo escrito en el párrafo previo, Cloranfenicol es un antibiótico adecuado en las siguientes indicaciones:
- Salmonelosis (fiebre tifoidea y paratifoidea).
- Rickettsiosis.
- Meningitis bacteriana por Haemophilus influenzae o meningococos.
- Infecciones no-meningocócicas por Haemophilus influenzae, sobre todo en niños, en particular epiglotitis, osteomielitis, celulitis y neumonía, sobre todo cuando derivan hasta sepsis.
- Abscesos cerebrales.
- Infecciones estafilocócicas.
- Infecciones por bacterias anaerobias Gram negativas.
- Infecciones por enterobacterias aerobias Gram negativas.
- Melioidosis, causada por Burkholderia pseudomallei (antes denominada: Pseudomonas pseudomallei).
- Infecciones bacterianas otológicas u oftalmológicas.
- Enfermedades venéreas, siempre como antibiótico de 2ª elección, siendo las tetraciclinas la primera opción (linfogranuloma venéreo y granuloma inguinal).
- Peste y tularemia.
- Fiebre recurrente transmitida por artrópodos (respuesta a una dosis única).
RESISTENCIA AL CLORANFENICOL
Se han descrito cuatro mecanismos de resistencia al Cloranfenicol: Por orden de importancia: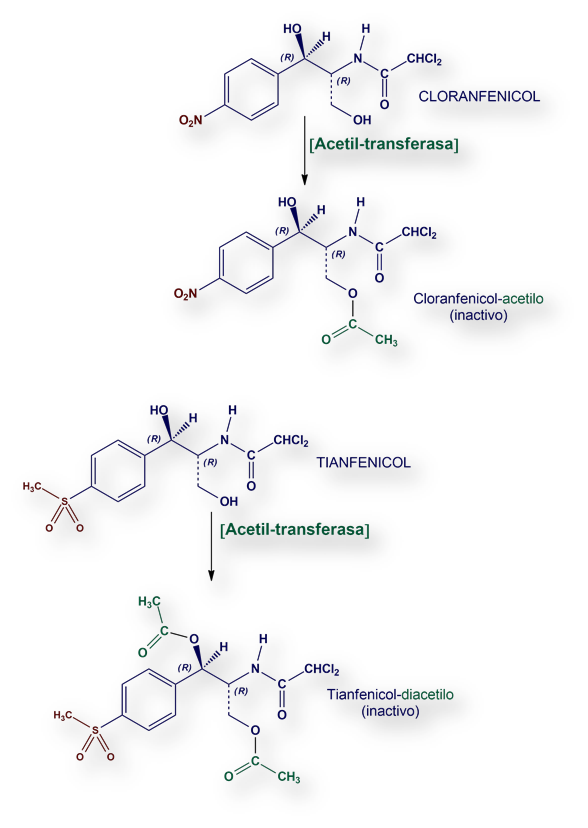 Resistencia transmitida por plásmidos. El gen del plásmido transfiere a la rickettsia una enzima con actividad «Cloranfenicol-acetil-transferasa» que añade uno (Cloranfenicol) o dos (Tianfenicol) grupos acetilo, anulando su actividad farmacológica de los antibióticos acetilados.
Resistencia transmitida por plásmidos. El gen del plásmido transfiere a la rickettsia una enzima con actividad «Cloranfenicol-acetil-transferasa» que añade uno (Cloranfenicol) o dos (Tianfenicol) grupos acetilo, anulando su actividad farmacológica de los antibióticos acetilados.
- Un segundo mecanismo de resistencia tiene que ver con la alteración de la permeabilidad bacteriana al antibiótico. Este mecanismo se ha descrito en Escherichia coli, Haemophilus influenzae y Pseudomonas aeruginosa.
- El tercer mecanismo de resistencia tiene que ver con la pérdida de una proteína de membrana de 50KD (50.000 unidades de masa atómica). El segundo y tercer mecanismo de resistencia parecen compartir un origen genético ancestral común.
- El cuarto mecanismo de resistencia es la inactivación del antibiótico mediante nitrorreducción. Se ha observado sobre todo en gérmenes anaerobios.
MECANISMO ACCIÓN
Ambos medicamentos (Cloranfenicol y Tianfenicol) actúan inhibiendo la enzima «peptidil-transferasa», más apropiadamente «aminoacil-RNA-transferasa», encargada de la adición de aminoácidos a la cadena proteica que se está sintetizando en el complejo ribosómico.
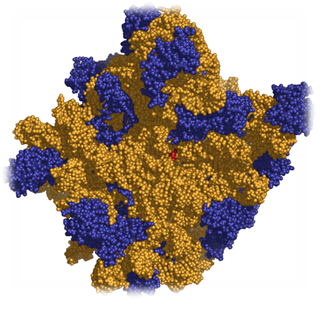 Los ribosomas bacterianos se distinguen de los ribosomas de las células eucariotas en sus coeficientes de sedimentación [en la ultracentrífuga], cuantificados mediante la letra S, patronímico de Theodor Svedberg, Premio Nobel de Química en 1926 en reconocimiento de sus investigaciones sobre la Química de los coloides.
Los ribosomas bacterianos se distinguen de los ribosomas de las células eucariotas en sus coeficientes de sedimentación [en la ultracentrífuga], cuantificados mediante la letra S, patronímico de Theodor Svedberg, Premio Nobel de Química en 1926 en reconocimiento de sus investigaciones sobre la Química de los coloides.
En un sentido amplio los ribosomas bacterianos tienen un coeficiente de sedimentación 70S, y los de las células eucariotas 80S. Esta diferencia es trascendente en el contexto de la acción antibiótica. [Obsérvese que los ribosomas mitocondriales son también 70S, hecho que, junto a otros hallazgos, hizo teorizar en el origen bacteriano de estos orgánulos sub-celulares].
Cada uno de los veinte aminoácidos tiene su propio transportador [ARN de transferencia] con actividad enzimática, de tal modo que cataliza la incorporación de un aminoácido a la cadena proteica en crecimiento, siguiendo el patrón del ARN mensajero. Simplificando en extremo, el proceso de elongación de la cadena peptídica transcurre mediante la transpeptidación, catalizada por la enzima «peptidil-transferasa», nombre genérico para las diferentes «aminoacil-RNA-transferasas». Este proceso tiene lugar en la unidad ribosómica 50S. De ahí que el mecanismo de acción del Cloranfenicol (y Tianfenicol) se atribuyan a la inhibición de la unidad ribosómica 50S.
Cloranfenicol (y Tianfenicol) se consideran bacteriostáticos (la síntesis ribosómica continúa cuando se remueve el antibiótico en estudios experimentales in vitro). No obstante, ambos antibióticos pueden ser bactericidas en función de la fase del ciclo celular. En la fase de rápida multiplicación la acción de estos antibióticos se puede catalogar de bactericida (se produce la lisis bacteriana); y durante los estadios de división más lenta la acción predominante es bacteriostática (la bacteria no muere pero no se multiplica), siendo el sistema inmune el encargado de su destrucción final (lisis bacteriana).
TOXICIDAD DEL CLORANFENICOL
Además del efecto más grave, antes comentado, de aplasia de la médula ósea, otros dignos de mención son los siguientes:
- Síndrome gris (en recién nacidos): es consecuencia de concentraciones tóxicas del antibiótico. La sintomatología cursa con distensión abdominal, vómitos, palidez, cianosis y colapso circulatorio. La mortalidad es muy elevada (> 50%). Debuta al cabo de entre 2 y 9 días de instaurar un tratamiento con Cloranfenicol, con hipotonía, letargia, color gris ceniza de la piel (de donde procede el nombre de síndrome gris), taquipnea o apnea, hipoperfusión periférica, hipotensión, hipotermia y acidosis. Además se observa alteración de la función cardíaca. La causa más probable es la inmadurez hepática de estos niños muy pequeños que tienen disminuida la conjugación del Cloranfenicol con ácido glucurónico – glucuronidación. Aunque muy raramente, el Síndrome gris también se ha notificado en adultos tratados con sobredosis de Cloranfenicol.
- Neuritis óptica. Se presenta fundamentalmente en niños con fibrosis quística tratados de modo crónico o frecuente con Cloranfenicol para sus infecciones pulmonares reiterativas. En algunos casos, la neuritis óptica degenera en atrofia óptica y ceguera irreversible. A veces, junto a la neuritis óptica, también se han producido otros síntomas neurotóxicos, tales como cefaleas, depresión, oftalmoplejia, confusión mental y delirios.
- Efectos adversos gastrointestinales: son mucho menos comunes que con las tetraciclinas. Aunque muy raramente, se han descrito casos de colitis pseudomembranosa, glositis y estomatitis.
- Ototoxicidad. Se ha notificado en niños que recibieron Cloranfenicol para tratar meningitis por Haemophilus influenzae en una formulación otológica (gotas) con una concentración >5%.
Aunque en la actualidad relegado a preparaciones farmacéuticas de uso otológico u oftalmológico, Cloranfenicol, junto a su hermano putativo Tianfenicol, son dos excelentes medicamentos, parte fundamental de la historia de la antibioticoterapia.
Zaragoza, a 14 de abril de 2020
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Florentino Ballesteros, 11-13
50002 Zaragoza
[1] De entre todos los microorganismos estudiados en la Naturaleza, solo algunos actinomicetos, eubacterias algunos hongos filamentosos segregan antibióticos. Solamente los actinomicetos sintetizan aproximadamente 6.000 sustancias (metabolitos) de los que alrededor de 1,500 tienen algún grado de actividad antibiótica, muchas veces demasiado débil para ser útiles farmacológicamente.
[2] Ehrlich J., et al. Chloramphenicol, a new antibiotic from soil actinomycetes. Science 1947; 106: 417.
[3] Bartz Q.R. Isolation and characterization of chloromycetin. J Biol. Chem. 1948; 172: 445-450.
[4] Controulis J., et al. Chloramphenicol (chloromycetin). Synthesis. J. Am. Chem. Soc. 1949; 71: 2463-2468.
[5] Botiger L. E. Drug induced aplastic anemia in Sweden with special reference to chloramphenicol. Postgrad Med J. 1974; 50(Suppl): 127-130.
[6] Wallerstein R.O., et al. Statewide study of chloramphenicol therapy and fatal aplastic anemia. J Am Med Assoc. 2008; 2045-2048.

