Un virus es poco más que un paquete de información que ha de replicarse de modo imperativo, pues de ello depende su supervivencia. Hasta hace pocos años los virus eran los gérmenes infecciosos más pequeños que se podía imaginar. La realidad siempre nos supera. ¿Recuerdan la «infección de las vacas locas», técnicamente encefalopatía espongiforme[1]? Las partículas infecciosas de las encefalopatía espongiformes son tan solo proteínas infecciosas, de donde procede su denominación de priones[2] (proteínas infecciones)[3].
Volvamos a los virus. Su manual de instrucciones es un ácido nucleico dirigido a la producción de nuevos virus a costa de convertir a la célula que infectan en esclava a su servicio, a la que, una vez explotada hasta la extenuación, terminan destruyendo. Es una estratagema perversa.
Hay quien cuestiona, no sin razón, que se pueda considerar a los virus verdaderos seres vivos. Por sí solos no pueden replicarse, desplazarse, crecer o perpetuarse.
Cuando un virus infecta una célula, toda la ingeniería bioquímica [de la célula] se pone su disposición. Desde ese momento, la única función de la célula es seguir el manual de instrucciones del virus (su ácido nucleico). La célula, condenada a muerte por anticipado, trabaja sin otro objetivo que producir nuevas partículas víricas. Se podría afirmar que la célula actúa a la manera de una fotocopiadora microscópica, sin otro destino final que su propia lisis
Desde hace seis meses, el coronavirus SARS-Covid-2 que comenzó modestamente causando unas pocas neumonías atípicas en una ciudad interior de la inmensa República Popular China, se ha extendido por todo el mundo. Su peaje está siendo devastador: más de seis millones de infectados (primeros días de junio de 2020) y, hasta ahora, alrededor de 370.000 muertos, si bien la cifra real es significativamente más elevada. Estados Unidos ha superado en dos meses los 100.000 muertos, una cuarta parte de todos los que murieron en los distintos frentes durante la Segunda Guerra Mundial. Otro aspecto de la tragedia es el económico: en apenas 10 semanas, 40 millones de estadounidenses han perdido su trabajo, en una sociedad no habituada al problema del desempleo; y los programas de ayuda alimentaria nos retrotraen a los años de la Gran Depresión durante la década de 1930. El virus ha alimentado la frustración generalizada y ha ensanchado la fractura social, destruyendo en tiempo record décadas de prosperidad solo atenuados por la Recesión de 2008-2012, generada por la codicia bancaria.
La llegada del verano al hemisferio norte (con mucho, el más densamente poblado) amortiguará la pandemia, tal vez haga que desaparezca. Sin embargo, algunos expertos dan por sentado que el Covid-19 (término de la infección causada por SARS-Covid-2) resurgirá el próximo otoño. Sería la segunda oleada; y todavía una tercera fase sería posible.
En un símil de fútbol, podríamos estar en el primer tiempo; falta el segundo, y tal vez una prórroga. Además, nuevos coronavirus podrían surgir, algunos con potencial pandémico.
El número de virus distintos es incalculable, ¿billones, trillones? Nadie lo sabe. Los virus infectan bacterias; pero también murciélagos, caracoles, escarabajos, gatos, perros, pangolines y hasta el denomino de Tasmania; causan cánceres en humanos y animales, incluso contribuyen al ennegrecimiento de la piel de los plátanos. En fin, son ubicuos. De los ¿billones? de virus existentes, alrededor de 7.000 están nominados; de éstos, tan solo de 250 son, hasta ahora, infecciosos para el hombre.
Hemos trivializado semánticamente a los virus (virus informáticos, comentarios virales en redes sociales). Pero ahora confrontamos un virus real, pandémico, capaz de alterar la vida social y económica del planeta hasta un grado difícil de imaginar hace apenas unos meses, aunque el riesgo de pandemia se venía previendo desde el año 2006. Se nos han hecho cotidianas palabras hasta que hasta hace poco tiempo nos eran ajenas: distanciamiento [social], confinamiento, cuarentena, y otras. La Naturaleza nos ha mostrado la insignificancia de nuestra especie resurgiendo con todo su esplendor, los animales (zorros, jabalíes) se han convertido en paseantes extemporáneos de nuestras desoladas avenidas. Las manifestaciones de afecto, las reuniones sociales, los viajes, los teatros, conciertos, cines e incluso los funerales han dejado de existir. La política busca refugio en la ciencia, pero ésta no puede tomar decisiones, solo exponer hechos sin respuesta; y la política convive mal con la falta de certidumbre.
 Se ha luchado por salvar las vidas de los enfermos probando a ciegas medicamentos obsoletos o inexperimentados. Apenas conocemos cómo mata el virus, por la escasez de autopsias. Con la escasa perspicuidad de los pocos meses de pandemia, parece como si la neumonía que afectó a los primeros casos se hubisese convertido en una enfermedad sistémica en la cual la afectación pulmonar es solo una de las manifestaciones clínicas. Se han iniciado con premura proyectos de investigación en busca de vacunas. Pero la ciencia y la prisa son pésimos compañeros de viaje.
Se ha luchado por salvar las vidas de los enfermos probando a ciegas medicamentos obsoletos o inexperimentados. Apenas conocemos cómo mata el virus, por la escasez de autopsias. Con la escasa perspicuidad de los pocos meses de pandemia, parece como si la neumonía que afectó a los primeros casos se hubisese convertido en una enfermedad sistémica en la cual la afectación pulmonar es solo una de las manifestaciones clínicas. Se han iniciado con premura proyectos de investigación en busca de vacunas. Pero la ciencia y la prisa son pésimos compañeros de viaje.
La sociedad se ha enfrentado entre el temor y la responsabilidad. Los sanitarios han demostrado probidad y sacrificio. Cuando se redacta este texto el colectivo sanitario ha sido galardonado con el premio Princesa de Asturias.
No se conoce el origen de los virus. Se teoriza que evolutivamente comenzaron como microbios de vida libre que, a través de la selección natural se fueron simplificando desde si complejidad inicial hasta convertirse en microbios dependientes de otros (en este caso células) para su supervivencia. O tal vez, surgieron a partir del propio ADN o ARN celular llegando a convertirse en entidades independientes.
Como se ha escrito antes, los virus son poco más que un manual de instrucciones, en forma de ácido nucleico (ADN de doble hélice, o ARN unicatenario). Asociadas al ácido nucleico hay pequeño número de proteínas, imprescindibles para invadir a las células que infectan y para su propia replicación.
En relación al tamaño medio de los virus, el SARS-Covid-2 es relativamente grande. Es de mayor tamaño que el virus ébola. Con todo, es minúsculo: su diámetro es la diezmilésima parte de 1mm, la milésima parte del ancho de un cabello humano; más pequeño incluso que la longitud de onda de la luz de una lámpara germicida.
El coronavirus causante de la actual pandemia se identificó formalmente el 7 de enero (2020) en la República Popular China, varias semanas después de que apareciesen los primeros casos de una neumonía atípica en la megalópolis de Wuhan, provincia de Hubei. En un principio se creyó que se trataba del resurgimiento del coronavirus que entre los años 2002 y 2003 causó el SARS (Severe Acute Respiratory Syndrome), una enfermedad que debuto con gran alarma, pero que no adquirió una extensión global (pandémica). Infectó a 8.098 personas en 20 países de los que fallecieron 774 (algo menos de un 10%). Se desarrolló una vacuna que no llegó a utilizarse porque la infección desapareció de modo tan sorpresivo como surgió.
Pronto se evidenció que el virus causante de la entonces aún denominada neumonía de Wuhan era un coronavirus. Era el tercer coronavirus que causaba un problema de salud importante en el siglo XXI, tras el SARS de 2002-2003, y el MERS[4] de 2013 del que todavía se notifican algunos casos esporádicos, sin duda el más peligroso si adquiriese una expansión pandémica (su mortalidad es de aproximadamente el 35% de los infectados).
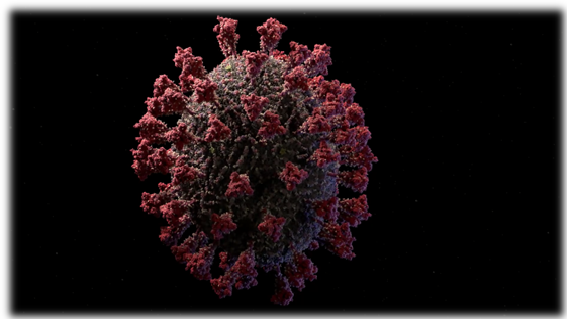
June Almeida, un técnico de laboratorio escocesa, visualizó por primera vez un coronavirus bajo la ampliación de un microscopio electrónico en 1966, cuando trabajaba en un hospital canadiense. Los describió como una corona solar, de donde surgió el nombre de coronavirus.
Años atrás denominábamos las epidemias y pandemias con sintagmas más literarios: «gripe española», «gripe asiática», «fiebre amarilla», «muerte negra»; ahora codificamos los nombres: SARS-CoV-1, gripe H1N1, MERS-CoV, HIV (causante del SIDA); códigos de letras como los códigos de los propios virus.
El 11 de febrero, el International Committee on Taxonomy of Viruses clasificó al actual virus pandémico como SARS-CoV-2. La Organización Mundial de la Salud designó a la enfermedad como Covid-19. La razón era la gran homología genómica (~97%) con el coronavirus de SARS-CoV-1 (causante de la epidemia del bienio 2002-2003).
Existen cientos de coronavirus: de ellos, los causantes del SARS (CoV-1 y el actual CoV-2), junto al que da lugar al MERS pueden ser mortales; otros (HCov 229E, NL63, OC43 y HKU1) solo desencadenan un elevado porcentaje de los resfriados comunes; los hay que afectan a animales domésticos y salvajes; y todos parecen convivir con (y en) los murciélagos.
Todos los coronavirus contienen ARN como ácido nucleico.
El código genético (el manual de instrucciones) del coronavirus SARS-Covid-19 contiene la información codificada para la síntesis de no menos de 29 proteínas. Una de estas proteínas (S, del inglés Spike, espiga) sobresale del núcleo del virus y es la responsable de la interacción con un tipo de receptor de las células que posibilita que el virus penetre en la célula. Una vez que el virus ha invadido la célula el ARN se aplica a su tarea: dividirse y, con la ayuda indispensable de la maquinaria celular, sintetizar el conjunto de proteínas que, tras su ensamblaje en el aparato de Golgi[5], darán lugar a nuevas partículas víricas (viriones).
De modo más concreto, la proteína S del SARS-Covid-2 se engarza con un receptor de la célula humana designado ACE2 (acrónimo de Angiotensin Convertase Enzyme type 2). La proteína vírica S es casi idéntica (la misma secuencia de aminoácidos) que su homóloga del coronavirus SARS-Covid-1 (causante de la epidemia del bienio 2002-2003). Sin embargo, la unión proteína S↔ receptor ACE2 es mucho más fuerte en el actual coronavirus que en el primer coronavirus SARS. ¿Radica en este hecho su mayor infectividad? A la luz de los conocimientos actuales, no existe una respuesta.
Una de las razones de la proliferación pandémica del SARS-Covid-2 es que la persona contagiada es transmisora de la infección varios días antes de que debuten sus síntomas. No sucedía así con el coronavirus de 2002-2003. El coronavirus SARS-Covid-1 causaba tos y fiebre en los pacientes desde el primer momento, alertando de su presencia. Ello ayudó a controlar su expansión. En cambio, el SARS-Covid-2 es muy sibilino: infecta primero la nariz, garganta y tracto respiratorio superior, sin apenas causar síntomas. De hecho, durante este ínterin es más contagioso. Cuando aparecen los síntomas (respiratorios y de otro tipo) su contagiosidad disminuye.
Además existen personas con una mayor densidad de receptores ACE2 en las células epiteliales del tracto respiratorio más profundo, siendo más propensas a la manifestación de la enfermedad pulmonar en su forma más grave y con mayor compromiso vital. Los minúsculos alveolos donde se produce el intercambio gaseoso entre el O2 y el CO2 se inflaman y colapsan. La tensión de oxígeno del enfermo (determinada mediante un pulsioxímetro) disminuye, señal de que los tejidos no reciben el suficiente oxígeno para su metabolismo. El paciente entra en el estado de hipoxia, con sensación de ahogo[6]. En este estadio es preciso el soporte vital mediante un ventilador mecánico.
 Durante estos meses de pandemia se ha observado que el virus puede dañar las paredes musculares del corazón y los vasos sanguíneos, dando lugar a coagulopatías y accidentes cerebrovasculares (ictus), nefropatías y encefalopatías. No obstante, la propia reacción inmunitaria a la infección puede ser más peligrosa para la supervivencia del enfermo que el propio virus con la expresión ya popularizada de «tormenta de citoquinas».
Durante estos meses de pandemia se ha observado que el virus puede dañar las paredes musculares del corazón y los vasos sanguíneos, dando lugar a coagulopatías y accidentes cerebrovasculares (ictus), nefropatías y encefalopatías. No obstante, la propia reacción inmunitaria a la infección puede ser más peligrosa para la supervivencia del enfermo que el propio virus con la expresión ya popularizada de «tormenta de citoquinas».
Si bien en un comienzo la sintomatología de los primeros pacientes parecía ceñirse a un proceso neumónico respiratorio (tos y disnea fundamentalmente) acompañado de fiebre, más tarde se han añadido una pléyade de síntomas: cansancio extremo, dolores generalizados, anorexia, anosmia (pérdida del sentido del olfato), disgeusia (pérdida o modificación del sentido del gusto), alteraciones vasculares, muy graves en ocasiones (trombosis, ictus), incluso convulsiones y delirios (a consecuencia de las encefalopatías) y otros todavía cuestionados.
Según la revista Science, se trata de un patógeno como nunca se haya visto antes. Además, mientras tiene una mortalidad algo superior al 5% (estimación todavía muy aproximada), hasta un 35% de infectados son asintomáticos, aunque contagiosos.
Caso de no haberse tomado medidas de aislamiento social este virus podría infectar a toda la Humanidad.
El 10 de enero (2020) la comisión de salud de la ciudad de Wuhan (República Popular China) informó a la Organización Mundial de la Salud que durante las semanas previas 41 personas habían enfermado de una neumonía atípica, de las que 1 había muerto. Era el 10 de enero. Hoy, cuatro meses después, hay más de 6 millones de afectados en todo el mundo, de los que más de 300.000 han fallecido (valores estimativos, muy probablemente a la baja).
Ese mismo día (10 de enero) científicos de Shanghái pusieron a disposición de todo el mundo el genoma completo del virus. Esta información estuvo disponible en varios servidores, entre otros: www.bioRxis.org y www.virological.org
Desde ese momento, el virus comenzó a replicarse, en las células humanas y en los temores de una sociedad planetaria desprevenida ante lo que se mostraba una pandemia, con imprevisibles efectos sanitarios y económicos.
Con tantas proteínas en su kit de herramientas, el virus tiene muchas maneras de contrarrestar nuestro sistema inmunológico. Cada una de estas herramientas [del virus] es una diana para los potenciales anticuerpos (vacunas). Una de las proteínas (antígenos) más atractivos para desarrollar una vacuna son las proteínas S (Spike), las primeras que interactúan con las células que van a ser infectadas. Parece como si el virus desactivase inicialmente nuestro sistema inmune; y éste, en una reacción ulterior, muchas veces desmedida, atacase al virus con tanta virulencia que termina matando al virus y ¡al paciente!
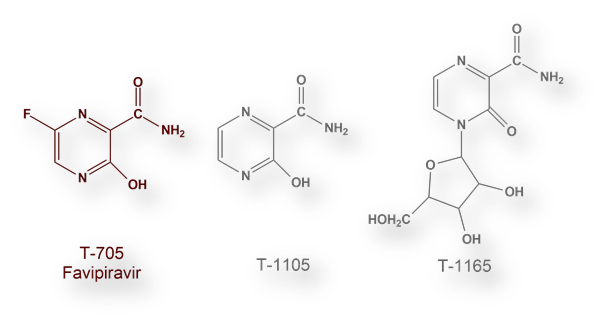
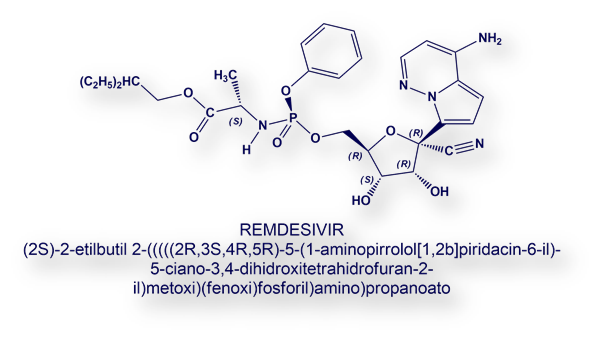
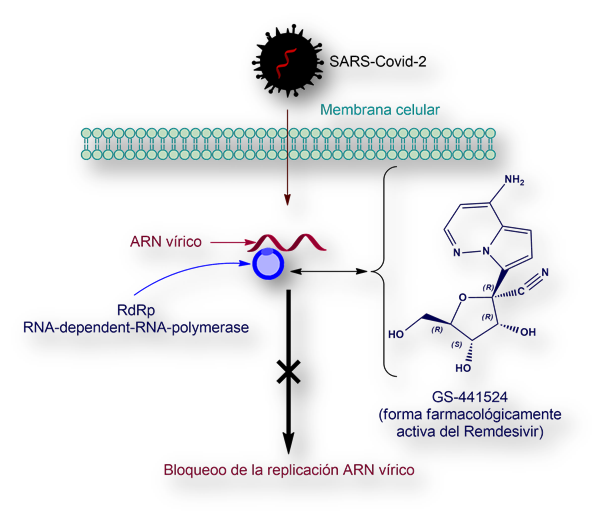
Hasta ahora los medicamentos que se han mostrado más eficientes, dentro de que no se han diseñado específicamente para esta infección, son Remdesivir y EIDD-2801. Ambos actúan bloqueando la replicación del virus (duplicación del ARN vírico). Otros (APN01, TAK888, y diversos cócteles de anticuerpos monoclonales) impiden la entrada del virus en la célula; y, un tercer grupo (Sarilumab, Tocilizumab, Tofacitinib y Remestencel-L) intentan refrenar la excesiva reacción inmunitaria[7]).
Otra línea de investigación es conocer cómo los distintos componentes sintetizados en la célula se ensamblan para formar nuevas partículas víricas. Esta investigación se entronca en otra más amplia sobre el tráfico intracelular de proteínas en el aparato de Golgi y la exocitosis (salida de los nuevos virus formados de las células) en la búsqueda de nuevas células a las que infectar.
Desde hace varias generaciones la Humanidad no ha confrontado un situación como la actual. La sociedad debería tomar conciencia de su vulnerabilidad, reflexionar y anticiparse a un futuro incierto e imprevisible.
Zaragoza, a 5 de junio de 2020
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Zaragoza
[1] Espongiforme se debe a que examinando post-mortem el cerebro de los fallecidos remedaba una esponja, llena de oquedades.
[2] Stanley B. Prusiner recibió el Premio Nobel de Fisiología o Medicina en 1977 por el descubrimiento de los priones.
[3] Las enfermedades priónicas incluyen la enfermedad de Creuzfeldt Jakob, kuru y la enfermedad de Gerstmann-Sträusser.
[4] MERS, acrónimo de Middle East Respiratory Syndrome.
[5] Camillo Golgi, ex aequo Santiago Ramón y Cajal recibieron el Premio Nobel de Fisiología y Medicina en el año 1906 por sus investigaciones sobre la estructura microscópica del sistema nervioso.
[6] Se han notificado pacientes hipóxicos sin disnea (insuficiencia respiratoria).
[7] El uso, muy controvertido, de la Cloroquina e Hidroxicloroquina, se fundamenta en su acción inmunosupresora, razón por la cual estos antiguos medicamentos antimaláricos se usan en algunas enfermedades auto-inmunes, sobre todo en el lupus eritematoso sistémico.