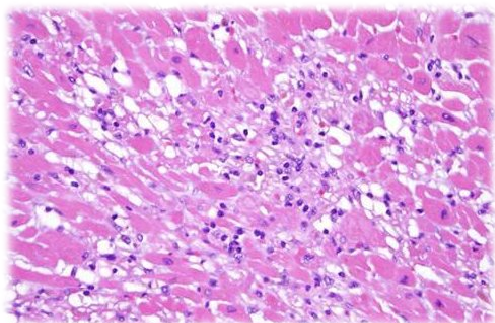
Imagen microscópica de tejido cardíaco proveniente de la necropsia de un paciente con melanoma que desarrolló un miocardiopatía mortal. Se observan células T (puntos azules) invadiendo y destruyendo fibras musculares cardíacas.
Los «inhibidores de PDL-1», también conocidos como «inhibidores de checkpoint» representan una esperanzadora estrategia farmacológica contra el cáncer. La experiencia clínica es, hasta ahora, muy limitada. Sin embargo, alrededor del 1% de los pacientes tratados han experimentado efectos tóxicos de tipo cardíaco que son una extensión indeseada del propio mecanismo de acción de estos fármacos, la activación del sistema inmunitario en su lucha contra el cáncer. Como se muestra en la fotografía, las células T (derivadas de los linfocitos T) se inmiscuyen en el tejido cardíaco destruyendo las fibras musculares. Se han notificado varias muertes por esta causa.
La yatrogenia de estos «inhibidores del checkpoint» aumenta cuando se toman dos medicamentos del mismo grupo simultáneamente.
Estos hallazgos se han publicado en la revista The New England Journal of Medicine, en un trabajo dirigido por Javid J. Moslehi, experto en cardiología y oncología en Vanderbilt School of Medicine.
La inmunoterapia no es, al menos por ahora, el talón de Aquiles del cáncer. Esta estrategia terapéutica funciona en algunos pacientes y tipos de cáncer.
Aun cuando los «inhibidores de checkpoint» se han autorizado para seis tipos de cáncer, se usan para otros muchos. Además, es común su asociación con otros medicamentos (quimioterapia clásica) para conseguir mejores respuestas clínicas.
Los casos comunicados de cardiotoxicidad son un inconveniente, pero no deben invalidar la investigación en este campo. Estos fármacos continúan ofreciendo un potencial anticanceroso poco frecuente.
Hasta ahora se han autorizado cuatro «inhibidores de checkpoint»: Ipilimumab (Yervoy®), Nivolumab (Opdivo®), Pembrolizumab (Keytruda®) y Atezolizumab (Tecentriq®).
Cuando se administran estos anticuerpos monoclonales se realizan pruebas de función cardíaca con el fin de anticiparse hasta donde sea posible a la potencial toxicidad cardíaca. Cuando se manifiesta cardiotoxicidad se instaura tratamiento con corticosteroides, aprovechando su capacidad de reprimir la respuesta inmunitaria.
Conforme aumenta el número de pacientes tratados con estos medicamentos, cabe prever que se comunicarán más casos de toxicidad cardíaca.
El primer «inhibidor del checkpoint» fue autorizado en el año 2011. Estos fármacos estimulan (sería mejor decir “des-reprimen”) a las células T para actuar contra las células cancerosas. [Muchos procesos neoplásicos inhiben el sistema inmunitario, una estrategia perniciosa que facilita su crecimiento]. Pero, en ocasiones, la reacción es desmedida, y las células T atacan a células de tejidos sanos. Se conocían estas reacciones sobre otros tejidos, tales como intestino, pulmón y glándula tiroides, pero no sobre el tejido cardíaco. Si bien se habían comunicado casos aislados de cardiotoxicidad en revistas médicas de poca influencia (bajo índice de impacto), esta es la primera vez que se publica un análisis exhaustivo, que incluye posibles causas, genéticas y/o virales (nunca encontradas), indagando en las bases de datos del fabricante (Bristol Myers Squibb) para detectar posibles casos no comunicados.
Los pacientes descritos en el artículo del Dr. Moslehi – una mujer de 65 años y un hombre de 63 – desarrollaron problemas cardíacos a las pocas semanas de la infusión intravenosa de dos «inhibidores de checkpoint» para tratamiento de melanomas. Ninguno tenía antecedentes de enfermedad cardíaca. Ambos pacientes terminaron falleciendo.
Los problemas cardíacos de la mujer debutaron con dolor torácico, disnea y fatiga. Ingresó en el hospital a los 12 días de haber recibido la primera inyección (infusión intravenosa) de los fármacos. La evolución de su cardiopatía condujo a miocarditis, miositis y arritmias. Al objeto de disminuir la inflamación muscular, sobre todo del miocardio, la paciente fue tratada con corticoides, pero el deterioro del corazón prosiguió irreversiblemente.
El caso del hombre fue posterior en el tiempo al de la mujer. Tras la experiencia adquirida con la paciente, se optó por usar dosis muy elevadas de corticoides, pero el paciente, aun cuando sobrevivió algunos días más, terminó falleciendo.
Las autopsias revelaron que el sistema inmune reaccionó contra el propio corazón como si fuese un xenotrasplante.
El grupo de estudio analizó las bases de datos del fabricante de ambos medicamentos (Bristol Myers Squibb). El número de pacientes que habían sido tratados con Yervoy® (Ipilimumab) y Opdivo® (Nivolumab) fue de 20.594. Se habían registrado 18 casos de miocarditis yatrogénica, de los que 6 fallecieron por esta causa; de éstos, 5 se produjeron en pacientes que habían sido tratados conjuntamente con ambos fármacos.
Un grupo de expertos dirigido por Michael B. Atkins, representante del Georgetown Lombardi Comprehensive Cancer Center, en Washington, se reunieron con ejecutivos de Bristol Myers Squibb en septiembre de 2016. Se acordó que los pacientes que vayan a recibir tratamiento con «inhibidores de checkpoint» hayan de someterse a electrocardiogramas, y hemogramas que incluyan la determinación de troponina, una proteína segregada por el miocardio dañado.
Los «inhibidores de checkpoint» son medicamentos trascendentes para muchos cánceres, si bien hasta ahora los ensayos se han centrado en el melanoma. Alrededor del 60% de los pacientes han de tratarse con ambos medicamentos (Ipilimumab y Nivolumab); y prácticamente se consiguen en todos los casos supervivencias prolongadas.
Antes de la existencia de estos «inhibidores de checkpoint» la supervivencia de los pacientes con melanoma era de seis a nueve meses; y menos de un 10% lograban sobrevivían dos años. La preocupación actual es conseguir que estos valiosos fármacos se puedan usar en condiciones fiables.
Algunas experiencias demuestran que es posible evitar que los pacientes desarrollen cardiopatías si se actúa con prontitud para desactivar el proceso inflamatorio derivado de la reacción de las células T contra los propios músculos del paciente, principalmente contra el miocardio.
Sin embargo, la actividad antiinflamatoria de los corticosteroides media a través de la inactivación de la respuesta inmune; y esto contrarresta el efecto terapéutico inherente a los «inhibidores del checkpoint».
Es pues necesario hallar algún marcador que haga posible discernir aquellos pacientes con elevada probabilidad de desarrollar cardiopatías con los «inhibidores de checkpoint». Pero, por ahora la única opción es monitorizar cuidadosamente los parámetros básicos de función cardíaca, incluyendo la troponina, muy especialmente cuando se recibe un tratamiento conjunto con Ipilimumab y Nivolumab.
Zaragoza, 9 de noviembre de 2016
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
FARMACIA LAS FUENTES
ZARAGOZA