En el año 1912 Frederick Gowland Hopkins sugirió que el raquitismo (véase fotografía de niños con piernas arqueadas y «pecho de paloma») podría estar causado por la falta de algún factor de la alimentación. Por sus hallazgos sobre la vitamina «anti-raquítica» Frederick Gowland Hopkins fue galardonado con el Premio Nobel de Fisiología o Medicina en 1929 ex aequo Christiaan Eijkman. [El reconocimiento a Christiaan Eijkman fue por su trabajo sobre la vitamina anti-neurítica o B1]. Externamente el raquitismo infantil da lugar a deformidad de los miembros debido a un déficit crónico de fosfato cálcico en los huesos en crecimiento.
El raquitismo, conocido desde tiempos antiguos, alcanzó proporciones casi de epidémicas a comienzos del siglo XIX y XX entre los niños de los suburbios de las grandes ciudades industriales que surgían en Europa y Norteamérica, debido a una pobre alimentación y una baja exposición a la luz solar durante los largos inviernos.
 Las consideraciones de Gowland Hopkins fue determinante para que el entonces recientemente formado Medical Research Committee se involucrase en el estudio de esta condición clínica. Tras varios experimentos con dietas restrictivas se descubrió que las grasas de origen animal, el [aceite de] hígado de bacalao y la mantequilla (no la margarina) tenían actividad «anti-raquítica».
Las consideraciones de Gowland Hopkins fue determinante para que el entonces recientemente formado Medical Research Committee se involucrase en el estudio de esta condición clínica. Tras varios experimentos con dietas restrictivas se descubrió que las grasas de origen animal, el [aceite de] hígado de bacalao y la mantequilla (no la margarina) tenían actividad «anti-raquítica».
De hecho, el aceite de hígado de bacalao formaba parte de muchos remedios populares en las tradiciones de los países del norte de Europa, donde se usaba, no solo para prevenir las deformidades óseas del crecimiento, sino para la tuberculosis y el reumatismo. Ya en el año 1861, Armand Trousseau, médico de la Clinique Médicale de L’Hôtel de Dieux (París) lo empleaba para prevenir el raquitismo. Sin embargo, este hallazgo empírico pasó desapercibido hasta los primeros estudios estandarizados a comienzos del siglo XX.
Hacia 1900 se creía que la vitamina «anti-raquítica» (más tarde se le designaría con la letra D, por ser la cuarta descubierta) y la vitamina A eran la misma sustancia. La equivocación se resolvería tras varios experimentos químicos en los que se evidenció la mayor labilidad de la vitamina A. Los extractos crudos sometidos a elevadas temperaturas perdían la actividad asociada a la vitamina A, pero mantenían la acción «anti-raquítica». Se trataba, pues, de entidades químicas distintas.
 En el año 1919 un médico berlinés, Kurt Huldschinsky demostró que se podía curar el raquitismo en niños cuando se les exponía a la luz ultravioleta producida por una lámpara de vapor de mercurio. Los resultados fueron confirmados en Viena por otro grupo de trabajo dirigido por Chick. Era el final de la Primera Guerra Mundial y la incidencia de raquitismo infantil en Viena era enorme.
En el año 1919 un médico berlinés, Kurt Huldschinsky demostró que se podía curar el raquitismo en niños cuando se les exponía a la luz ultravioleta producida por una lámpara de vapor de mercurio. Los resultados fueron confirmados en Viena por otro grupo de trabajo dirigido por Chick. Era el final de la Primera Guerra Mundial y la incidencia de raquitismo infantil en Viena era enorme.
Al otro lado del Atlántico, en New York, se teorizó que el factor «anti-raquítico» se producía por la acción de la radiación sobre una provitamina putativa presente en la piel
 El 19 de junio de 1922 el periódico The New York Times informaba que un equipo de investigación dirigido por E. V. McCollum había aislado una vitamina de un extracto con propiedades «anti-raquíticas». Se le denominó vitamina D: y cuando se administraba aisladamente prevenía el raquitismo infantil. Quedaba así demostrado que se trataba del «factor anti-raquítico».
El 19 de junio de 1922 el periódico The New York Times informaba que un equipo de investigación dirigido por E. V. McCollum había aislado una vitamina de un extracto con propiedades «anti-raquíticas». Se le denominó vitamina D: y cuando se administraba aisladamente prevenía el raquitismo infantil. Quedaba así demostrado que se trataba del «factor anti-raquítico».
Este hallazgo fue un hito en la Salud Pública. A partir de entonces numerosos gobiernos obligaron a reforzar los alimentos con vitamina D. Con esta medida se consiguió reducir drásticamente la prevalencia del raquitismo infantil.
 En junio de 1924 se descubrió que la irradiación solar de determinados alimentos les confería propiedades «anti-raquíticas». De hecho la Wisconsin Alumni Research Foundation (WARF) patentó este procedimiento, que generó durante los veinte años siguientes unas regalías superiores a los veinte millones de dólares, una cantidad impresionante para la época. La vitamina D producida mediante la irradiación de algunos alimentos era farmacológicamente idéntica a los esteroles extraídos de algunas plantas. [Como curiosidad un trascendente medicamento anticoagulante, la Warfarina debe su nombre al acrónimo WARF].
En junio de 1924 se descubrió que la irradiación solar de determinados alimentos les confería propiedades «anti-raquíticas». De hecho la Wisconsin Alumni Research Foundation (WARF) patentó este procedimiento, que generó durante los veinte años siguientes unas regalías superiores a los veinte millones de dólares, una cantidad impresionante para la época. La vitamina D producida mediante la irradiación de algunos alimentos era farmacológicamente idéntica a los esteroles extraídos de algunas plantas. [Como curiosidad un trascendente medicamento anticoagulante, la Warfarina debe su nombre al acrónimo WARF].
 Se sabía que una sustancia presente en la piel actuaba como pro-vitamina D. Su aislamiento se llevó a cabo en Göttingen bajo la dirección de Adolf Windaus. Al mismo tiempo se descubrió que una sustancia vegetal ya conocida, ergosterol, también era precursora de otra con actividad vitamina D. Adolf Otto Windaus recibió el Premio Nobel de Química en 1928 por sus investigaciones sobre los esteroles y su conexión con las vitaminas.
Se sabía que una sustancia presente en la piel actuaba como pro-vitamina D. Su aislamiento se llevó a cabo en Göttingen bajo la dirección de Adolf Windaus. Al mismo tiempo se descubrió que una sustancia vegetal ya conocida, ergosterol, también era precursora de otra con actividad vitamina D. Adolf Otto Windaus recibió el Premio Nobel de Química en 1928 por sus investigaciones sobre los esteroles y su conexión con las vitaminas.
En el año 1901, Adolf Otto Windaus, quien había trabajado en Berlín con Emil Fischer, comenzó su investigación sobre el colesterol y los esteroles (derivados del colesterol). Así mismo, estudió la conversión metabólica de la glucosa en proteínas; y subsidiariamente a esta investigación demostró la presencia de anillos imidazólicos en la estructura de las proteínas. Ello le llevó a descubrir que el aminoácido histidina es un derivado imidazólico de otro aminoácido, la alanina; y que la histamina tiene una estructura etilamina-imidazólica.
 Entre sus colaboradores se hallaba Adolf Butenandt, galardonado con el Premio Nobel de Química en el aciago año 1939 por sus investigaciones sobre las hormonas sexuales, también esteroles desde un punto de vista químico.
Entre sus colaboradores se hallaba Adolf Butenandt, galardonado con el Premio Nobel de Química en el aciago año 1939 por sus investigaciones sobre las hormonas sexuales, también esteroles desde un punto de vista químico.
[Adolf Butenandt recibió el Premio Nobel de Química ex aequo el croata Leopold Stephen Ruzicka, este último por sus trabajos sobre los poli-metilenos y los terpenos].
El interés de Adolf Otto Windaus por los esteroles le llevó a Estados Unidos, donde colaboró con Alfred Hess en el estudio de la vitamina «anti-raquítica».
Su otra rama de investigación le llevó a descubrir que la vitamina «anti-neurítica» (vitamina B1 o tiamina) tenía una estructura tiazólica y no imidazólica como inicialmente se creía.
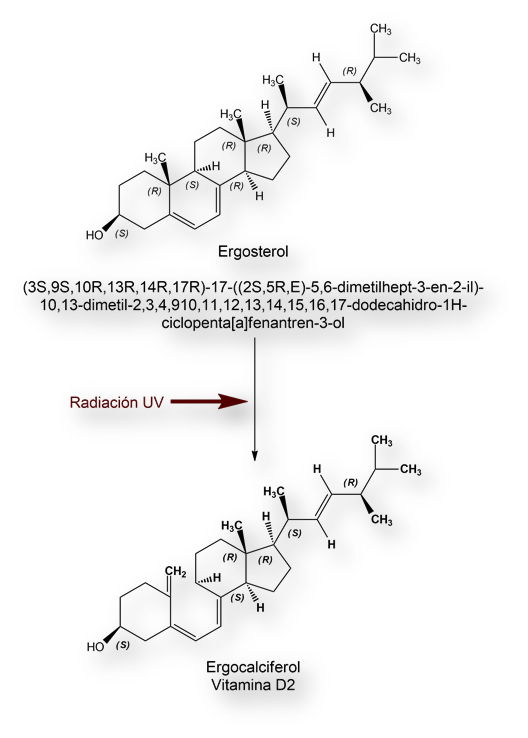
En colaboración con los laboratorios Elberfeld, parte integrante de I. G. Farbenindustrie, el grupo de trabajo dirigido por Adolf O. Windaus aisló en 1932 el producto formado por la irradiación del ergosterol. A este compuesto lo designó vitamina D2 para diferenciarlo de lo que creía se trataba de la verdadera vitamina, en la que esta molécula formaba un complejo con lumisterol, también un sub-producto de la irradiación del ergosterol. Al complejo (vitamina D2 y lumisterol) Adolf O. Windaus lo denominó vitamina D1. La estructura química de la vitamina D2 se dilucidó en el año 1936.
 Independientemente, en 1932, un grupo de investigación británico adscrito al National Institute for Medical Research de Londres, dirigido por Askew aisló el complejo vitamina D2, al que también se denominó ergocalciferol. Durante algunos años se consideró erróneamente que los preparados «británico» y «alemán» eran idénticos. Hoy día el sintagma vitamina D se usa como término genérico para describir cualquier sustancia que pueda convertirse en el organismo en el metabolito con actividad «anti-anti-raquítica» 1,25-dihidroxicolecalciferol (o: 1α, 25-ergocalciferol).
Independientemente, en 1932, un grupo de investigación británico adscrito al National Institute for Medical Research de Londres, dirigido por Askew aisló el complejo vitamina D2, al que también se denominó ergocalciferol. Durante algunos años se consideró erróneamente que los preparados «británico» y «alemán» eran idénticos. Hoy día el sintagma vitamina D se usa como término genérico para describir cualquier sustancia que pueda convertirse en el organismo en el metabolito con actividad «anti-anti-raquítica» 1,25-dihidroxicolecalciferol (o: 1α, 25-ergocalciferol).
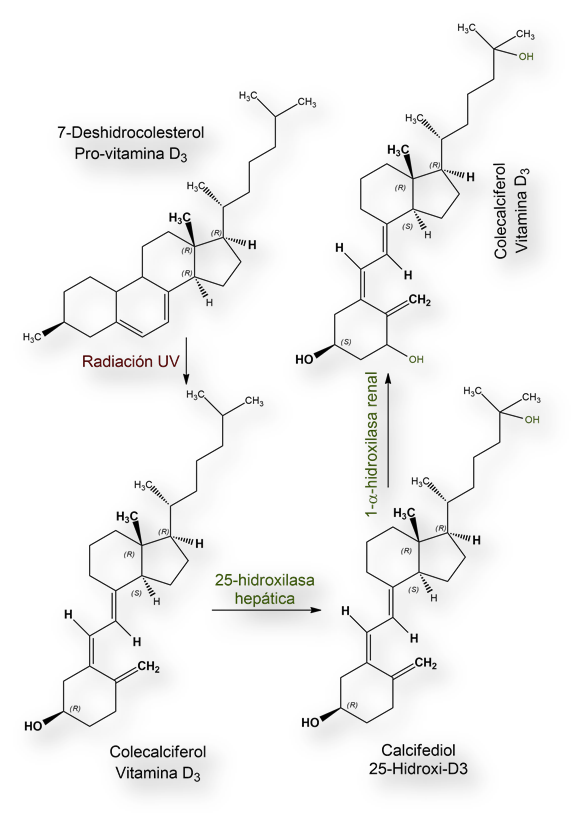
Adolf Otto Windaus descubrió también que otros esteroles presentes en la piel también generan metabolitos «anti-raquíticos» tras su activación por radiación solar. Así sucede cuando se sintetiza colecalciferol (vitamina D3) a partir del 7-deshidrocolesterol presente en la piel.
Colecalciferol (vitamina D3) fue sintetizada por el grupo de Hector DeLuca en la universidad de Wisconsin-Madison, Estados Unidos.
Además, Hector DeLuca identificó el calcifediol como el metabolito del colecalciferol. Debido a la mayor potencia y más rápido inicio de acción del Calcifediol (en relación al colecalciferol), se introdujo a partir de la década de 1970 para el tratamiento de la hipercalcemia en pacientes con hipoparatiroidismo primario y secundario (relacionado con diálisis).
 La vitamina D ejerce un trascendente papel en la homeostasis del calcio. Todos los mamíferos sintetizan pro-vitamina D de tal modo que en circunstancias normales la administración exógena como preparados farmacéuticos debería ser innecesaria. De hecho los receptores para la vitamina D se expresan en muchas células no involucradas en el metabolismo del calcio, tales como células hematopoyéticas, linfocitos, células epidérmicas, células de los folículos pilosos, células pancreáticas, adipocitos, neuronas y células musculares.
La vitamina D ejerce un trascendente papel en la homeostasis del calcio. Todos los mamíferos sintetizan pro-vitamina D de tal modo que en circunstancias normales la administración exógena como preparados farmacéuticos debería ser innecesaria. De hecho los receptores para la vitamina D se expresan en muchas células no involucradas en el metabolismo del calcio, tales como células hematopoyéticas, linfocitos, células epidérmicas, células de los folículos pilosos, células pancreáticas, adipocitos, neuronas y células musculares.
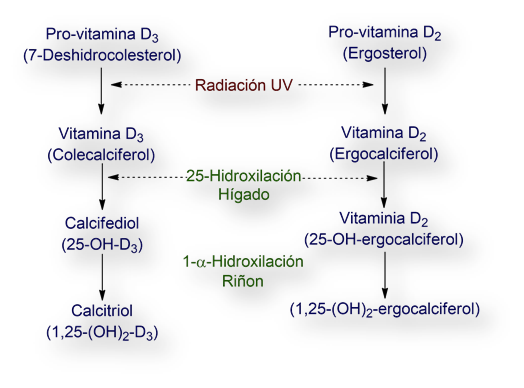
El sintagma vitamina D se aplica a dos sustancias liposolubles: colecalciferol (vitamina D3) y ergocalciferol (vitamina D2). Estos compuestos experimentan su modificación química (hidroxilaciones) hasta convertirse en metabolitos, que son responsables de la acción fisiológica. Las acciones biológicas se intermedian tras la interacción con un receptor específico, el cual fue clonado en 1987 (Science 1987; 235: 1214-1217).
La principal pro-vitamina hallada en la piel es 7-deshidrocolesterol. La radiación solar convierte el 7-deshidrocolesterol en colecalciferol (vitamina D3).
Por otra parte, el ergosterol, presente en plantas y hongos, difiere del 7-deshidrocolesterol (y su metabolito colecalciferol) en la presencia de un doble enlace C22-C23 y la presencia de un grupo metilo (-CH3) en C24. La mayoría de los preparados farmacéuticos contienen ergosterol, siendo también el compuesto que se genera tras la irradiación (enriquecimiento) del pan o la leche, fundamentalmente. En los humanos no hay diferencias de actividad «anti-raquítica» entre las vitaminas D2 y D3
 La vitamina D2 (ergocalciferol) se absorbe de modo preferencial en el intestino delgado; y en mucha menor cantidad en el yeyuno e íleo. La mayor parte de la fracción absorbida se integra en quilomicrones (complejas partículas grasas) en la linfa, desde donde pasa a la sangre (unido a la fracción proteica α-globulina). Se acumula en el tejido adiposo que, de esa manera, actúa como reservorio durante períodos prolongados.
La vitamina D2 (ergocalciferol) se absorbe de modo preferencial en el intestino delgado; y en mucha menor cantidad en el yeyuno e íleo. La mayor parte de la fracción absorbida se integra en quilomicrones (complejas partículas grasas) en la linfa, desde donde pasa a la sangre (unido a la fracción proteica α-globulina). Se acumula en el tejido adiposo que, de esa manera, actúa como reservorio durante períodos prolongados.
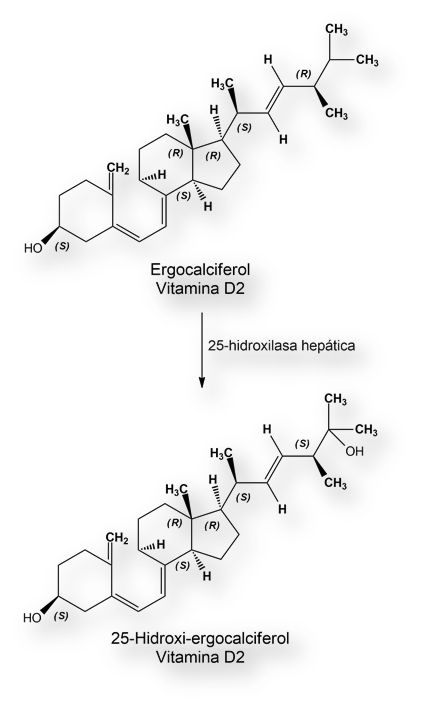
Tanto la vitamina D exógena (D2/ergocalciferol) como endógena (D3/colecalciferol) precisa modificación química (hidroxilaciones) para convertirse en las formas activas biológicamente. La primera etapa es la hidroxilación en C25. Esta primera hidroxilación tiene lugar en el hígado, formándose calcifediol (si se parte de la vitamina D2) o 25-hidroxi-ergocalciferol (si se parte de ergocalciferol). La T1/2 de ambas versiones de la vitamina D es de alrededor de 19 días, y las concentraciones en el estado de equilibrio (steady-state) se hallan en el rango 15 a 20ng/ml.
La segunda hidroxilación tiene lugar en el parénquima renal, formándose 1α, 25-dihidroxi-colecalciferol (calcitriol) o 1α.25-dihidroxi-ergocalciiferol.
Zaragoza, a 19 de enero de 2021
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Zaragoza

