Nancy Wexler con la fotografía de una mujer venezolana que participó en su investigación (1990)
Hay personas especiales que se comportan de modo excepcional. Una de ellas es Nancy Wexler. Durante años llevó equipamiento sanitario a remotas aldeas que circundan el lago Maracaibo en el noroeste de Venezuela donde afligía de modo casi epidémico una extraña enfermedad a la que llamaban el baile de Maracaibo o sencillamente «el mal». La enfermedad remedaba al baile San Vito, razón por que a los afectados se les denominaba sanviteros. Los habitantes de las aldeas costeras del lago Maracaibo suelen vivir en palafitos sobre los humedales. La enfermedad, hoy se sabe hereditaria, causa degeneración cerebral y discapacidad progresiva irreversible y mortal. El médico venezolano Américo Negrette describió la sintomatología durante su trabajo en la región entre los años 1952 y 1956. Se trata de la enfermedad de Huntington.
Junto a los movimientos coreicos (antiguamente se denominaba Corea de Huntington), los enfermos sufrían graves alteraciones de su patrón de sueño, con profunda somnolencia diurna, y ensoñaciones trágicas o eróticas. Todos los enfermos sufrían intensas cefaleas, un pródromo de la enfermedad. Un hecho común son las frecuentes e inexplicables caídas. Un paciente le describió a Américo Negrette: “es como si las piernas se escapasen de mí”. Las caídas al comienzo de la enfermedad son un signo premonitorio de rápida progresión de la enfermedad neurodegenerativa. En las mujeres, la sintomatología empeoraba coincidiendo con la menstruación, menopausia, embarazo o tras un aborto, provocado o espontáneo.
Otros aspectos descritos por Américo Negrette eran los profundos cambios conductuales, los más notorios la depresión, angustia e irascibilidad. Negrette definió los cambios psicológicos como una especie de intuición mórbida que les conducía a un estado de resignación profundamente triste, sabedores de que la enfermedad era incurable e irremisiblemente mortal. Reproduzco un párrafo de su libro sobre la Corea de Huntington:
Los coreicos no eligen sus hábitos ni su estilo de vida. Solo pueden vivir la vida tal como se les presenta. Casi todos fuman. Algunos beben [en exceso]. Los matrimonios legales están limitados y suelen engendrar muchos niños. Cuando un miembro de la pareja desarrolla la enfermedad el otro miembro de la pareja abandona a la familia; la mujer abandona al hombre, que sucumbe a su infortunio en soledad; el hombre deja a su esposa junto con los numerosos niños en la más absoluta pobreza. Sus problemas de carácter son tan manifiestos que ningún coreico puede aspirar a encontrar una pareja sana.
Al infortunio de los enfermos se añade su marginación social, al considerar, aun hoy día, que están afectados de una enfermedad contagiosa. Los médicos locales los evitan; los sacerdotes también. Nancy Wexler, junto a Américo Negrette creó, partiendo de la total inexistencia, una mínima infraestructura sanitaria en que los enfermos pudieran hallar alivio, médico y afectivo.
Nancy Wexler consiguió interesar a científicos de prestigio en la investigación de esta enfermedad, patronímica del médico estadounidense George Huntington, quien la describió por primera vez en el año 1872.
Las investigaciones Nancy Wexler y otros investigadores, continuadores de las primeras y dramáticas descripciones de Américo Negrette, condujeron al descubrimiento del gen responsable de esta enfermedad, así como al hallazgo de otros genes que actúan como moduladores del gen responsable.
Ahora, a sus 74 años, Nancy Wexler ha hecho pública una amarga noticia, conocida sotto voce por sus colaboradores: ella misma tiene la enfermedad que con tanto entusiasmo investigó; la misma que causó la muerte a muchos miembros de su familia.
Entre sus principales preocupaciones continúan estando las familias venezolanas afectadas por la enfermedad de Huntington. Gracias a estas infortunadas familias se obtuvieron muestras de sangre, piel, y cerebro de congéneres fallecidos, que fueron primordiales para descifrar la genética de la enfermedad.
Sin embargo, estas personas pertenecen a comunidades muy pobres. La clínica que Nancy Wexler construyó en la región del lago Maracaibo ha sido cerrada por los actuales gobernantes bolivarianos.
El hecho de que su familia [de Nancy Wexler] porte la mutación de Huntington crea con esas gentes un vínculo afectivo muy especial.
Si los tratamientos experimentales que se están ensayando en la actualidad funcionan, los enfermos venezolanos deberían recibirlos de modo gratuito, tal como escribió en una editorial de la revista médica The New England Journal of Medicine).
Aun cuando hasta ahora Nancy Wexler no había explicitado su condición de portadora de la mutación de Huntington, sus colegas científicos conocían su circunstancia porque los signos y síntomas clínicos eran evidentes: caminar inestable, disartria, movimientos involuntarios de cabeza y tronco, y un carácter con brotes de irascibilidad. Precisa un andador para moverse fuera de su departamento en la universidad de Columbia, en New York. Sus limitaciones físicas, cada vez más graves, no han condicionado su fortaleza mental, ni aminorado su capacidad de trabajo.
Nancy Wexler ha colaborado en el desarrollo de un fármaco, un «oligonucleótido anti-sentido» que podría estar disponible hacia el año 2022, en función de los resultados logrados durante los ensayos clínicos, de los que ella, dada su edad, no se podrá beneficiar.
Existe el precedente del Nusinersen (Spinraza®), un «oligonucléotido anti-sentido» para el tratamiento de la Atrofia Muscular Espinal, enfermedad para la que también se han desarrollado dos vanguardistas tratamientos: Risdiplam, el primer medicamento per os que modifica un proceso genético; y Zolgensma® (Onasemnogene abeparvovec xioi) la primera terapia génica.
Parte de la historia personal de Nancy Wexler se narra en un documental, todavía no estrenado (abril 2020), de Ken Burns y Barak Goodman, titulado «The Gene».
El espectro de la enfermedad ha estado presente en su vida desde que cumplió 22 años, en 1968. Su madre, Leonor Wexler y sus tres hermanos habían muerto como consecuencia de la enfermedad de Huntington. La dramática experiencia familiar le indujo a estudiar genética, siempre con la esperanza de hallar alguna solución a la terrible enfermedad.
Las mutaciones del gen HTT, ubicado en el cromosoma 4, causan la enfermedad de Huntington. Este gen codifica la síntesis de una proteína denominada huntingtina, cuya función fisiológica se ignora, si bien su importancia se infiere de las terribles consecuencias de su incorrecto funcionamiento.
- Nucleótidos:
- C: Citosina
- A: Adenina
- T: Timina
- G: Guanina
- Aminoácidos:
- His: histidina
- Ser: serina
- Gln: glutamina
- Ile: isoleucina
- Val: valina
- Leu: leucina
- Met: metionina
La mutación HTT involucra a un segmento de ADN denominado triplete repetitivo CAG (Citosina, Adenina, Guanina). Este codón aparece repetido un significativo número de veces, entre 30 y 35 en el gen HTT. En las personas con mutación de Huntington, el número de repeticiones es superior, de 36 a 120 repeticiones. Las personas que tienen entre 36 y 39 repeticiones no desarrollarán la clínica de la enfermedad, pero sí aquellas con 40 o más repeticiones del triplete (codón) CAG.
Un aumento del número de repeticiones dará lugar a la síntesis de una proteína (huntingtina) más larga, con secuencias de poli-glutamina (el codón CAG codifica la síntesis del aminoácido glutamina). La hidrólisis de la proteína (huntingtina) da lugar a fragmentos más largos, que forman agregados muy tóxicos para las neuronas. La disfunción, seguida de la muerte neuronal, desencadena los signos y síntomas de la enfermedad de Huntington.
La genopatía de Huntington se hereda siguiendo un patrón autosómico (no ligado al sexo) dominante (un único alelo mutado causa la enfermedad, con gravedad variable en función del número de repeticiones del triplete CAG). Si el número de repeticiones del triplete CAG en el gen HTT está en el rango 40 a 50, la enfermedad debuta en edad adulta; si el número de repeticiones supera las 60 la enfermedad de Huntington se inicia durante la adolescencia o primera adultez. Cuanto mayor es el número de repeticiones del triplete CAG en el gen HTT la enfermedad debuta a edades más tempranas, y su prognosis es peor.
Los afectados heredan la mutación de uno de los progenitores. Muy raramente, la enfermedad surge por una mutación «de novo» (sin herencia parental).
De sólito, la enfermedad de Huntington suele manifestarse en la tercera o cuarta década de vida, cuando la mayoría de las personas ya han procreado. Tal fue el caso de la madre de Nancy Wexler en quien la genopatía debutó muy tardíamente, a la edad de 53 años.
Al inicio de la enfermedad la depresión, irritabilidad y otras alteraciones psicológicas y psiquiátricas son manifiestas. Los pacientes pierden su capacidad de hablar (afasia), mientras son plenamente conscientes de su deterioro.
La enfermedad de Huntington se encuadra entre las enfermedades raras. Según algunas estimaciones, hay alrededor de 4.000 personas en España diagnosticados de enfermedad de Huntington; y alrededor de 15.000 en espera de padecerla.
La historia de Nancy Wexler es dramática. Al conocer su diagnóstico, su madre trató de suicidarse. Su esposo (padre de Nancy Wexler) lo evitó, si bien declaró haberse arrepentido más tarde tras observar el deterioro físico y mental de su esposa y el sufrimiento asociado. Tardó 10 años en fallecer a consecuencia de las complicaciones.
Tras la muerte de su madre, Nancy Wexler viajó por primera vez a Venezuela a fin de estudiar a una familia numerosa tras la descripción de su caso por Americo Negrette, Era el año 1955. Parecía tratarse de la familia con la mayor prevalencia mundial de enfermedad de Huntington. El ADN de los miembros de esta familia fue trascendental para descubrir el gen involucrado en la enfermedad y la investigación farmacológica que puede llevar al primer fármaco «oligonucléotido anti-sentido».
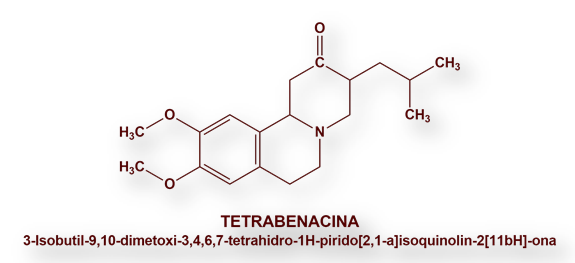 En la actualidad se recurre a la Tetrabenazina como único fármaco que parece paliar los movimientos coreicos, uno de los signos clínicos más llamativos de la enfermedad.
En la actualidad se recurre a la Tetrabenazina como único fármaco que parece paliar los movimientos coreicos, uno de los signos clínicos más llamativos de la enfermedad.
La Tetrabenacina incrementa la actividad serotoninérgica cerebral. En un experimento se inyectó a animales clorofenilalanina (una sustancia inhibidora de la síntesis de 5-hidroxitriptamina). La inyección subsiguiente de 30mg/Kg de Tetrabenacina mostró acción sedante sobre la actividad locomotora, consecuencia de la recuperación de la actividad serotoninérgica cerebral.
Adjunto la página web de la Hereditary Disease Foundation, creada por el padre de Nancy Wexler y continuada por ella misma.
Cuando Nancy Wexler y sus colegas científicos llegaron a las aldeas ribereñas del lago Maracaibo, hallaron a muchos pacientes, incluidos algunos niños, con la enfermedad que las gentes denominaban “el mal”. Nancy Wexler les explicó que ella también padecía la enfermedad y les animó a dejarse extraer pequeñas muestras de piel, tal como ella misma había realizado. Casi por primera vez, alguien extranjero, además del médico venezolano Américo Negrette, trataba a estas personas con dignidad, no como apestados.
A lo largo de los años el equipo de trabajo de Nancy Wexler recogió más de 4.000 muestras de sangre, y trazó un árbol genealógico de 10 generaciones que incluía a más de 18.000 personas.
Dedicar con esfuerzo y ahínco su vida profesional a estudiar la misma terrible enfermedad que ella padece la convirtió en un referente, no solo entre sus colegas científicos, sino entre las pobres gentes de la región venezolana en la que «el mal», como lo siguen llamando, tenía (y tiene) una elevada prevalencia. [Américo Negrette falleció en septiembre de 2003].
En el año 1983, tan solo cuatro años después del primer viaje a la región del lago Maracaibo, se descubrió un marcador, un fragmento de ADN próximo al gen buscado, que finalmente se localizó en el cromosoma 4. Este hallazgo representó un hito en la genética clínica.
El padre de Nancy Wexler, psicoterapeuta de personajes del mundo del espectáculo, usó su influencia para la obtención de financiación para la fundación, Hereditary Disease Foundation.
El descubrimiento del gen permitió desarrollar una prueba genética que permite conocer si se es portador del gen mutado. Sin embargo, la determinación genética plantea un dilema ético, dado que hoy día no existe tratamiento. Tal vez la única razón que justifique su realización es evitar que los afectados tengan descendencia a la que condenarían a una terrible e irreversible enfermedad.
Zaragoza, a 3 de abril de 2020
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Florentino Ballesteros, 11-13
50002 Zaragoza


