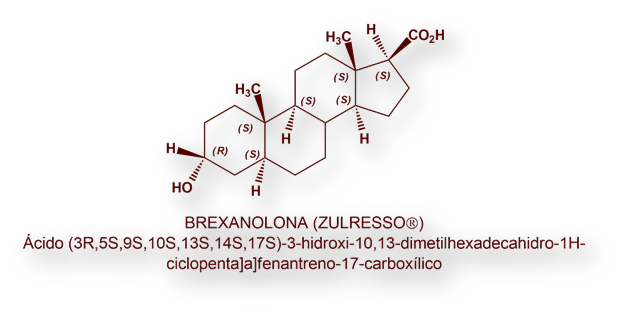
La Food and Drug Administration de Estados Unidos (US-FDA) ha autorizado (18 de marzo de 2019) la comercialización del primer medicamento para el tratamiento de la depresión postparto. Se trata de brexanolona con nombre de fantasía Zulresso®.
 Brexanolona se administra en infusión intravenosa continua durante 60 horas (2,5 días), bajo estricta supervisión debido al riesgo de sedación excesiva, incluso pérdida de conciencia, observada durante los ensayos clínicos. La mejoría es perceptible dentro de las primeras 48 horas tras instaurar la infusión intravenosa. Ello ha motivado que brexanolana se haya de administrar dentro del programa REMS (Risk Evaluation and Mitigation Strategy). El programa REMS está pensado para tratamientos en que hay que contrapesar cuidadosamente los beneficios vs riesgos. Se instauró inicialmente para los tratamientos con opiáceos.
Brexanolona se administra en infusión intravenosa continua durante 60 horas (2,5 días), bajo estricta supervisión debido al riesgo de sedación excesiva, incluso pérdida de conciencia, observada durante los ensayos clínicos. La mejoría es perceptible dentro de las primeras 48 horas tras instaurar la infusión intravenosa. Ello ha motivado que brexanolana se haya de administrar dentro del programa REMS (Risk Evaluation and Mitigation Strategy). El programa REMS está pensado para tratamientos en que hay que contrapesar cuidadosamente los beneficios vs riesgos. Se instauró inicialmente para los tratamientos con opiáceos.
Es difícil establecer una prevalencia fiable de la depresión postnatal, todavía muy estigmatizado socialmente, pues parece contranatural el desapego de una madre hacia su hijo. Según algunas estimaciones 1 de cada 7 mujeres desarrollan este un cuadro sintomático de depresión postparto de gravedad variable. Los síntomas que sirven para su diagnóstico incluyen una sensación de tristeza, desesperanza y profundo abatimiento, exteriorizado mediante llanto incontrolable; ansiedad, irritabilidad, inquietud, insomnio o somnolencia, pérdida (pasajera) de memoria, falta de concentración, dificultades ejecutivas (toma de decisiones en aspectos básicos), anhedonia (imposibilidad de disfrutar con actividades placenteras), somatizaciones (cefaleas, dolor epigástrico, mialgias); retraimiento (rechazo de familiares y amigos), anorexia o bulimia, incapacidad de llevar a cabo los cuidados básicos del bebé; y, en los casos más graves, tendencias criminales hacia su hijo, o autodestructivos (ideaciones suicidas).
La infusión de brexanolona tendrá un coste muy elevado (34.000 dólares) por paciente, con independencia de los descuentos que pueda establecer el fabricante (Sage Therapeutics) con las compañías aseguradoras. A este precio hay que añadir los derivados del ingreso hospitalario durante al menos 2,5 días. Las compañías de seguros privados en Estados Unidos todavía no se han manifestado acerca de la cobertura, total o parcial, del tratamiento.
Una presentación oral de una molécula similar (denominación preclínica SAGE-217) se halla actualmente en fase de ensayos clínicos. Su precio podría ser sustancialmente más bajo, pero su comercialización se demorará, en el mejor de los casos, un par de años.
La infusión de brexanolona se administra una sola vez. Las pacientes deben ser tratadas simultáneamente con un antidepresivo clásico («inhibidor de la recaptación de serotonina», o «inhibidor mixto [de recaptación de serotonina y noradrenalina]»).
Los ensayos clínicos con brexanolona han sido financiados por el fabricante (SAGE Therapeutics) y dirigidos por Samantha Meltzer Brody, directora del Programa de psiquiatría perinatal de la universidad de North Caroline, en Chape Hill, Estados Unidos. En uno de ellos (Brexanolona injection in post-partum depression: two multicentre, doublé-blind, randomised, placebo-controlled, phase 3 trials) se evidenció mejoría significativa.
El efecto terapéutico conseguido se mantenía un mes después de finalizada la infusión intravenosa de brexanolona. No hay evidencia de mejorías a más largo plazo, si bien algunos informes no contrastados refieren beneficios terapéuticos prolongados.
Los ensayos clínicos incluyeron a 247 mujeres seleccionadas al azar. Se distribuyeron de manera aleatoria en dos grupos, tratados respectivamente con placebo (infusión de solución salina fisiológica) o brexanolona disuelta en solución salina fisiológica. El número de participantes fue escaso en relación con ensayos clínicos estándar. Ello no obstante, los comités de la Food and Drug Administration consideraron el año pasado (2018) que los resultados fueron suficientemente persuasivos para recomendar la aprobación de brexanolona en el tratamiento de la depresión postparto refractaria a la farmacoterapia antidepresiva convencional. La decisión se tomó casi por unanimidad.
Las mujeres que participaron en los ensayos clínicos habían dado a luz dentro de los seis meses anteriores, habiendo desarrollado un grave cuadro depresivo, bien durante el último trimestre de su gestación, o poco después del alumbramiento. Se excluyeron a las mujeres con psicosis o enfermedad bipolar. Las participantes podían tener ideaciones suicidas, pero se descartaron a quienes habían intentado suicidarse.
A pesar de que la brexanolona no se excreta en la leche materna, a las mujeres se les conminó a que dejasen la lactancia durante la infusión (60 horas) y los días posteriores.
La gran ventaja de la brexanolona es que el beneficio clínico es inmediato (apenas dos días) desde que se instaura la infusión intravenosa.
Con independencia de otras consideraciones, la autorización de brexanolona (Zulresso®) abre el camino a otros posibles tratamientos para este síndrome (depresión postparto o postnatal) para el que no se disponía de tratamiento efectivo.
En opinión de algunos psiquiatras, el tratamiento puede ser resolutivo para el 30% aproximadamente de todas las mujeres con depresión postparto.
Las candidatas al tratamiento serían aquellas mujeres que no consiguiesen una remisión de su cuadro depresivo postparto con la farmacoterapia antidepresiva convencional. Además de la necesidad de ingreso hospitalario, el principal problema deriva del precio de la infusión (34.000 US$ como valor promedio).
Algunas mujeres que participaron voluntariamente en el ensayo clínico declararon haber logrado un rápido alivio de sus incapacitantes síntomas depresivos pudiendo reducir la dosis del antidepresivo oral con que estaban siendo tratadas.
Durante los ensayos clínicos los efectos adversos más referidos fueron el mareo y la somnolencia (1 de cada 8 mujeres tratadas). Sin embargo, el efecto adverso más importante es la excesiva sedación que puede llegar a pérdida de conciencia. Durante los ensayos clínicos, este efecto se notificó en 5 mujeres. Todas se recuperaron al cabo de 1 hora, continuando la administración de brexanolona.
Brexanolona se está estudiando para el status epilepticus (ensayos fase 3, habiendo recibido la Fast Track Designation por la FDA), y para el temblor esencial (ensayos fase 2).
 La brexanolona es una forma sintética de alopregnanolona, un metabolito de la progesterona, modulador del receptor GABAA.
La brexanolona es una forma sintética de alopregnanolona, un metabolito de la progesterona, modulador del receptor GABAA.
Alopregnanolona disminuye la respuesta cerebral al «factor liberador de corticotropina», péptido hormonal que desempeña una trascendente función en la respuesta al estrés. Este descubrimiento se dio a conocer el 10 de noviembre de 2004 en la revista Journal of Neuroscience (Progesterone Attenuates Corticotropin-Releasing Factor-Enhanced But Not Fear-Potentiated Starties via Activity of Its Neuroactive Metabolite, Allopregnanolone). Este hallazgo representó un acicate para la búsqueda de potenciales medicamentos con que tratar la ansiedad y depresión en mujeres. ¿El primer psicofármaco «de género»?
Zaragoza, a 21 de marzo de 2019
Dr. José Manuel López Tricas
Farmacéutico especialista Farmacia Hospitalaria
Farmacia Las Fuentes
Florentino Ballesteros, 11-13
50002 Zaragoza

